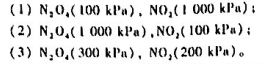题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
298.15K时,某N2(g)分子在α=0.2196m的立方体势箱中运动,其第一激发态与基态的能级差Δɛ=()J.
298.15K时,某N2(g)分子在α=0.2196m的立方体势箱中运动,其第一激发态与基态的能级差Δɛ=()J.
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“298.15K时,某N2(g)分子在α=0.2196m的立方…”相关的问题
更多“298.15K时,某N2(g)分子在α=0.2196m的立方…”相关的问题
可逆反应 达到化学平衡时:
达到化学平衡时:
(1)升高温度,反应标准平衡常数(),其原因是();
(2)在温度不变的条件下压缩气体的体积而增大压力时,I(g)的解离度().其原因是();
(3)恒容条件下充入N2,I2(g)的解离度(),其原因是()。
(4)恒压条件下充入N2,I2(g)的解离度(),其原因是()。
1000K时,反应C(s)+2H2(g) CH4(g)的A,Gf=19290/mol.现有与碳反应的气体,其中含有CH.(g)10%,H2(g)80%,N2(g)10%(体积%)。试问:
CH4(g)的A,Gf=19290/mol.现有与碳反应的气体,其中含有CH.(g)10%,H2(g)80%,N2(g)10%(体积%)。试问:
(1)T=1000K,p=100kPa时,甲烷能否形成?
(2)在(1)的条件下,压力需增加到多少。上述合成甲烷的反应才可能进行?
已知298.15K时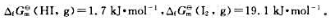 则化学反应
则化学反应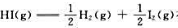 在298.15K时标准摩尔吉布斯自由能变
在298.15K时标准摩尔吉布斯自由能变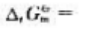 (),在标准状态下反应向方向自发进行。
(),在标准状态下反应向方向自发进行。
已知可逆反应: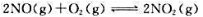 在298.15K下进时的
在298.15K下进时的 计算该可逆反应的标准平衡常数。在298.15K时,当反应系统中
计算该可逆反应的标准平衡常数。在298.15K时,当反应系统中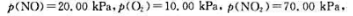 判断反应进行方向。
判断反应进行方向。
已知298.15K时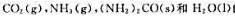 的标准摩尔生成焓和标准摩尔熵如下表所示:
的标准摩尔生成焓和标准摩尔熵如下表所示:

试通过计算判断下列反应
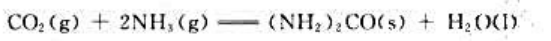
在298.15K、标准状态下能否自发进行。上述反应在标准状态下自发进行的最高温度是多少?
已知四氧化二氮的分解反应如下:

在298.15K时,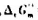 =4.75kJ·mol-1.试判断在此温度及下列条件下,反应进行的方向.
=4.75kJ·mol-1.试判断在此温度及下列条件下,反应进行的方向.