 更多“(1£«2)HCl溶液是把2体积的浓盐酸溶于1体积水而成的溶…”相关的问题
更多“(1£«2)HCl溶液是把2体积的浓盐酸溶于1体积水而成的溶…”相关的问题
-1之间时,溶液的总体积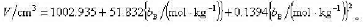
求:
(1)把水(A)和醋酸(B)的偏摩尔体积分别表示成bB的函数关系。
(2)bB=L.5mol·kg-1时水和醋酸的偏摩尔体积。
质量分数为36.0%的浓盐酸(密度1.19),其物质的量浓度C(HCL)为()。(注:HCL分子量为36.5)
A.42.84mol/L
B.36.0mol/L
C.12.06mol/L
D.11.74mol/L
快溶液解,然后发生歧化反应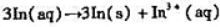 每间隔一定时间分析溶液中余下的c(In+),有关实验数据如表3-6.
每间隔一定时间分析溶液中余下的c(In+),有关实验数据如表3-6.

(1)画出ln{c(In+)}图,确定该反应的速率系数和速率方程;
(2)确定反应的半衰期.
下列情况,有无沉淀生成?
(1)0.001mol·L-1Ca(NO3)2溶液与0.0lmol·L-1NH4HF2溶液以等体积相混合;
(2)0.01mol·L-1MgCl2溶液与0.1mol·L-1NH3-1mol·L-1NH4Cl溶液等体积相混合.
(1)每升碱液吸收了多少克CO2?
(2)用该碱液滴定某一元弱酸,若浓度仍以0.1026ml·L-1计算,会引起多大误差?
A.1℅
B.2℅
C.0.5℅
A.KCl、HBr、HI
B.HCl、H2SO4、H3PO4
C.KOH、NaOH、Ca(OH)2
D.HCl、CH3COOH、NH3·H2O
计算下列溶液的pH
(1)50℃纯水和100℃纯水;
(2)0.20mol·L-1HClO4;
(3)4.0x10-3mol·L-1Ba(OH)2;
(4)将S0mL0.10mol·L-1HI稀释至1.0L;
(5)将100mL2.0x10-3mol·L-1HCl和400mLI.0x10-3mol·L-1HCIO2混合;
(6)混合等体积的0.20mol·L-1HCI和0.10mol·L-1NaOH;
(7)将pH为8.00和10.00的NaOH溶液等体积混合;
(8)将pH为2.00的强酸和pH为13.00的强酸碱溶液等体职混合.


 如果结果不匹配,请
如果结果不匹配,请 
















