 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知ψϴ(Cu2+/Cu)=0.342V;ψϴ(I2/I-)=0.536V;ψϴ(Fe3+/Fe2+)=0.771V;ψϴ(Sn4+/Sn2+)=0.151V,判断下列还原剂的还原性由强到弱的是()
A、CuI-Fe2+Sn2+
B、I-Fe2+Sn2+Cu
C、Sn2+CuI-Fe2+
D、Fe2+Sn2+I-Cu
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A、CuI-Fe2+Sn2+
B、I-Fe2+Sn2+Cu
C、Sn2+CuI-Fe2+
D、Fe2+Sn2+I-Cu
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知ψϴ(Cu2+/Cu)=0.342V;ψϴ(I2/I-)…”相关的问题
更多“已知ψϴ(Cu2+/Cu)=0.342V;ψϴ(I2/I-)…”相关的问题
已知电池Cu|Cu2+(a2)||Cu2+(a1)|Cu和Pt|Cu2+(a2),Cu+(a')||Cu2+(a1),Cu+(a')|Pt的电动势分别为E1和E2,则( )
A.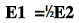 B.E1=2E2C.E1=E2D.E1≥E2
B.E1=2E2C.E1=E2D.E1≥E2
已知:EΘ(Ag+/Ag)=0.799V,EΘ(Cu2+/Cu)=0.340V,将反应2Ag++Cu=2Ag+Cu2+组成原电池,EΘ=________V。
A.Fe2+;
B.Cu
C.Mg
D.Cl-
298K时,在Ag+/Ag电极中加入过量I-,设达到平衡时c(I-)=0.1mol·dm-3,而另一电极为Cu2+/Cu,c(Cu2+)=0.01mol·dm-3,将两电极组成原电池,写出原电池符号、电池反应,并求电池反应平衡常数。
已知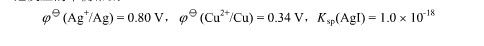
求下列电池的电动势: (一)Cu|[Cu(NH3)4]2+(0.10 mol.L-1),NH3(1.0 mol.L-1)‖Ag+(0.010 mol.L-1)|Ag() (已知Eθ(Ag+/Ag)=0.799 V,Eθ(Cu2+/Cu)=0.337 V,K稳θ[Cu(NH3)4]2+=4.8×1012)
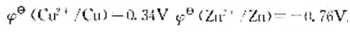 ,求此时原电池的电动势比标准状态时的电动势()
,求此时原电池的电动势比标准状态时的电动势()A.上升0.24V
B.下降0.24V
C.上升0.12V
D.下降0.12V
00mol/L),计算滴定至化学计量点时的pCu+和pCu值(已知lgKCuY=18.8,pH=10.0时,lgαCu(OH)=0.8,lgαY(H)=0.5,Cu-NH3配合物的各数累积常数lgβ1~lgβ4:4.13、7.61、10.48、12.59)
某溶液中含有1.00 mol·kg-1的Zn(NO3)2和1.00 mol·kg-1的Cu(NO3)2,pH=4.0,该溶液在25℃时,用光滑的Pt片作为电极。试问当阴极电势达-0. 30 V时,阴极上发生什么反应?这时溶液中残余Cu2+的浓度为多少?已知H2在光滑Pt片和Cu片上的超电势分别为0.1V和0.2v,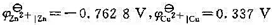 .假设不考虑其活度因子的影响。
.假设不考虑其活度因子的影响。
电池Cu|Cu+||Cu+,Cu2+|pt和电池Cu|Cu2+||Cu2+,Cu+|Pt的反应均写成Cu+Cu2+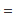 2Cu+,此两电池的( )。
2Cu+,此两电池的( )。

电池(-)Cu|Cu+||Cu+,Cu2+|Pt()和(-)Cu|Cu2+||Cu+,Cu2+|Pt()的反应均可写为 ,则此二电池的
,则此二电池的

