 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A-B-683 4 2 3某溶液主要含有Ca2+、Mg2+及少量的Fe3+、Al3+,在pH=10 时,加入三乙醇胺,以络黑T为指示剂,用EDTA滴定,测出的是()
A.Mg2+的含量
B.a2+的含量
C.e3+的含量
D.a2+和Mg2+的总量
 答案
答案
D、a2+和Mg2+的总量
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.Mg2+的含量
B.a2+的含量
C.e3+的含量
D.a2+和Mg2+的总量
 答案
答案
D、a2+和Mg2+的总量
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“A-B-683 4 2 3某溶液主要含有Ca2+、Mg2+及…”相关的问题
更多“A-B-683 4 2 3某溶液主要含有Ca2+、Mg2+及…”相关的问题
A.Mg2+含量
B.Ca2+含量
C.Ca2+和Mg2+总量
D.Fe3+和Al3+总量
E. Al3+、Fe3+、Ca2+、Mg2+总量
A.Mg2+ 量
B.Ca2+ 量
C.Ca2+、Mg2+ 总量
D.Ca2+、Mg2+ 、Fe3+、Al3+总量
A、Ca2+的含量
B、Ca2+、Mg2+总量
C、Mg2+的总量
D、Ca2+、Mg2+、Al3+、Fe3+的总量
A.Ca2+含量
B.Mg2+含量
C.Ca2+、Mg2+含量
D.Ca2+、Mg2+、Fe3+、Al3+总量
A.Ca2+的含量
B.Mg2+的含量
C.a2+、Mg2+、Fe2+、Al3+的总量
D.Ca2+、Mg2+的总量
为了测定水中Ca2+,Mg2+的含量,以下消除少量Fe3+,Al3+干扰的方法中,正确的是()。
A.于pH=10的氨性溶液中直接加入三乙醇胺
B.于酸性溶液中加入KCN,然后调至pH=10
C.于酸性溶液中加入三乙醇胺,然后调至pH=10的氨性溶液
D.加入三乙醇胺时,不需要考虑溶液的酸碱性
A.于酸性溶液中加入KCN,然后调制pH=10
B.于pH=10的氨性溶液中直接加入三乙醇胺
C.于酸性溶液中加入三乙醇胺,然后调至pH=10的氨性溶液
D.加入三乙醇胺时,不需要考虑溶液的酸碱性
用EDTA滴定Ca2+、Mg2+含量,以下消除少量Fe3+和A13+干扰的方法中,哪一种是正确的()。
A.在pH=10的氨性溶液中直接加入三乙醇胺
B.于酸性溶液中加入KCN,然后调至pH=10
C.于酸性溶液中加入三乙醇胺,然后调至pH=10的氨性溶液
D.加入三乙醇胺,不需要考虑溶液的酸碱性
A.(H+)/c(OH-)=1×1014的溶液:Ca2+、Na+、ClO-、NO3-
B.能与Al反应产生H2的溶液中:HCO3-、Na+、Al3+、Br-
C.使甲基橙变红的溶液:K+、Fe2+、SO42-、NO3-
D.常温下pH=1的溶液中:Mg2+、Cl-、SO42-、Fe3+
利用化学原理可以对工厂排放的废水、废渣等进行有效检测与合理处理。某工厂对制革工业污泥中Cr(Ⅲ)的处理工艺流程如下:其中硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+,Al3+,Ca2+,Mg2+。
(1)实验室用18.4mol·L的浓硫酸配制480mL4.6mol·L的硫酸,需量取浓硫酸()mL,配制时所用玻璃仪器除量筒、烧杯和玻璃棒外,还需()。
(2)酸浸时,为了提高浸取率可采取的措施有()。答出两点。
(3)H2O2的作用是将滤液Ⅰ中的Cr3+转化为Cr2O72-,写出此反应的离子方程式()。
(4)常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下: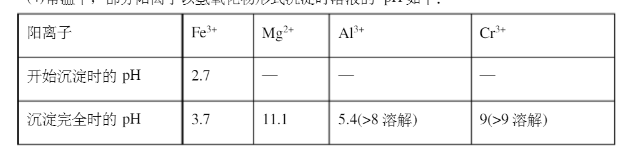 加入NaOH溶液使溶液呈碱性,既可以除去某些杂质离子,同时使Cr2O72-转化为CrO42-,但溶液的PH不能超过8,其理由是用离子方程式表示()。
加入NaOH溶液使溶液呈碱性,既可以除去某些杂质离子,同时使Cr2O72-转化为CrO42-,但溶液的PH不能超过8,其理由是用离子方程式表示()。
(5)钠离子交换树脂的反应原理为Mn++nNaR→MRn+nNa+,利用钠离子交换树脂除去滤液Ⅱ中的金属阳离子是()。
(6)写出上述流程中用SO2进行还原时发生反应的化学方程式:()。