 更多“属于吗啡的的前药,过量或长期使用易产生成瘾性的是()”相关的问题
更多“属于吗啡的的前药,过量或长期使用易产生成瘾性的是()”相关的问题
高铁酸钾是一种高效的多功能的水处理剂。工业上常采用NaClO氧化法生产,原理为:3NaClO+2Fe(NO3)3+10NaOH=2Na2FeO4↓+3NaCl+6NaNO3+5H2O Na2FeO4+2KOH=K2FeO4+2NaOH 主要的生产流程如下: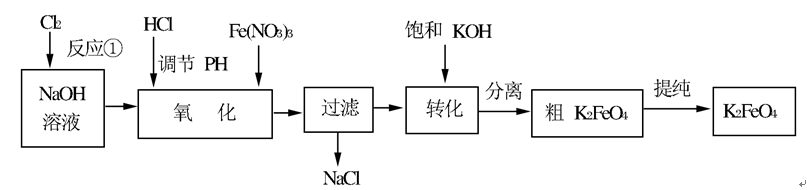 问题一、写出反应①的离子方程式()。
问题一、写出反应①的离子方程式()。
问题二、流程图中“转化”是在某低温下进行的,说明此温度下Ksp(K2FeO4)()Ksp(Na2FeO4)〔填“>”或“<”或“=”〕。
问题三、反应的温度、原料的浓度和配比对高铁酸钾的产率都有影响。
图1为不同的温度下,Fe(NO3)3不同质量浓度对生成率的影响;
图2为一定温度下,Fe(NO3)3质量浓度最正确时,NaClO浓度对K2FeO4生成率的影响
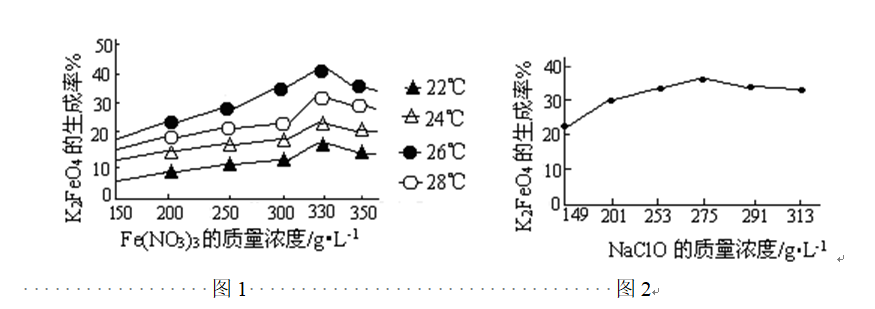
①工业生产中最正确温度为()℃,此时Fe(NO3)3与NaClO两种溶液最正确质量浓度之比为()。
②假设NaClO加入过量,氧化过程中会生成Fe(OH)3,写出该反应的离子方程式:()。假设Fe(NO3)3加入过量,在碱性介质中K2FeO4与Fe3+发生氧化复原反应生成K3FeO4,此反应的离子方程式:()。
问题四、K2FeO4在水溶液中易水解:
4FeO42—+10H2O 4Fe(OH)3+8OH—+3O2↑。在“提纯”K2FeO4中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用溶液()(填序号)。
4Fe(OH)3+8OH—+3O2↑。在“提纯”K2FeO4中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用溶液()(填序号)。
AH2O
BCH3COONa、异丙醇
CNH4Cl、异丙醇
DFe(NO3)3、异丙醇
A.是苯二氮类药物过量的特效解毒剂
B.作用时间较短,用于长效苯二氮类药物中毒需反复用药
C.对于长期使用或滥用苯二氮类药物而出现药物耐受的患者可安全使用
D.可逆转苯二氮类药物过量导致的镇静状态
A.作用弱,起效较慢长期使用不易产生耐药
B.与β2受体激动剂合用,尤其适用于夜间哮喘及痰多患儿
C.不良反应少可引起口腔干燥与苦
D.每次250—500ug,用药间隔同β受体激动剂
A.装斗前的中药饮片必须符合国家药品标准炮制的规定,末经炮制或炮制不合格的不能装斗
B.坚持“三查三对”的原则,对号入座
C.坚持先进先出,先产先出"的原则
D.饮片装斗应留有余地
E.中药饮片装斗加药前,必须对药斗及容器进行清洁处理,特别是盛装富炙饮片的容器,必须对内部站附的物质物定清洗,擦试


 如果结果不匹配,请
如果结果不匹配,请 
















