 更多“向酸性FeCl3溶液中通入H2S能形成Fe2S3沉淀。()”相关的问题
更多“向酸性FeCl3溶液中通入H2S能形成Fe2S3沉淀。()”相关的问题
解释实验现象。
(1)在煤气灯上加热KNO3晶体时没有棕色气体生成,但若KNO3晶体混有CuSO4时则有棕色气体生成。
(2)向KNO3的酸性溶液中加入Co(Ⅱ)盐,生成的K3[Co(NO2)6]沉淀中Co为+3价。
(3)向Na3PO4溶液中滴加AgNO3溶液时生成黄色沉淀,但向NaPO3溶液中滴加AgNO3溶液时却生成白色沉淀。
(4)向Na2HPO4溶液中加入CaCl2溶液有白色沉淀生成,但向NaH2PO4溶液中加入CaCl2溶液没有沉淀生成。
(5)分别向NaH2PO4,Na2HPO4和Na3PO4溶液中加入AgNO3溶液时,均得到黄色的Ag3PO4沉淀。
(6)向FeCl3溶液中滴加Na3PO4溶液,先有黄色沉淀生成;继续滴加时沉淀减少,最后消失得无色溶液。
(7)使AsH3通入一玻璃管,并在入口处加热,这时管壁出现有金属光泽的黑色物质。
(8)向含有Bi3+和Sn2+的澄清溶液中加入NaOH溶液会有黑色沉淀生成。
(9)将NaOH溶液与BiCl3溶液充分混合有白色沉淀生成,再向其中通入Cl2时有黄棕色沉淀生成。
在H3AsO3的稀溶液中通入H2S气体,生成As2S3溶胶。已知H2S能解离成H+和HS-。试写出As2S3胶团的结构,比较电解质AICl3,MgSO4和KCl对该溶胶聚沉能力大小。
A.0.51
B.0.45
C.0.15
D.0.13
推理判断:
(1)将白色固体化合物(A)加热,生成(B)和(C)。白色固体(B)可以溶于稀盐酸生成(D)的溶液,再向其中滴加适量氢氧化钠生成白色沉淀(E),氢氧化钠过量时沉淀消失。(C)是(F)的酸酐,浓酸(F)与单质硫作用生成有刺激性气味的气体化合物(G)和水,稀酸(F)与金属锌作用生成化合物(A)。
试给出(A),(B),(C),(D),(E),(F)和(G)的化学式,并完成各步的化学反应方程式。
(2)向化合物(A)的水溶液中,通入硫化氢气体,生成黑色沉淀(B),(B)经过过氧化氢处理转化成(C)。离心分离后将白色沉淀物(C)加热分解,得到(D)和(E)。(D)与氧化钡反应生成白色固体(F),(F)不溶于水,也不溶于稀硝酸。(E)与稀硝酸反应又生成(A)。(A)受热分解得黄色固体化合物(E),
试给出(A),(B),(C),(D),(E)和(F)的化学式,并完成各步的化学反应方程式。
(3)向化合物(A)的水溶液中,滴加一种钠盐(B)的溶液,先生成白色沉淀(C),(B)的溶液过量时沉淀消失生成(D),继续加入少许盐酸,产生有刺激性气味的气体(E)和黑色沉淀(F),同时体系呈乳白色浑浊状,表示有单质(G)生成。离心分离后固体物质(F)和(C)一同与过量稀硝酸共热,形成的溶液比(A)的溶液多出一种离子(H),因此可以与氯化钡反应生成白色沉淀(I);向清液中加入氯化钡溶液,亦有(I)生成,(I)不溶于稀硝酸。白色沉淀(C)不稳定,与水共存时有(F)和(H)生成。
试给出(A),(B),(C),(D),(E),(F),(G),(H)和(I)的化学式,并完成各步的化学反应方程式。
溶液(C)。将(B)溶于盐酸后经蒸发、浓缩析出(A)。向(A)的稀盐酸溶液中加入H2S溶液生成橙色沉淀(D)。(D)与Na2S2可以发生氧化还原反应,反应产物之间作用得到无色溶液(E)。将(A)投入水中生成白色沉淀(F)。试给出(A),(B),(C),(D),(E)和(F)所代表的物质的化学式,并用化学反应方程式表示各过程。
下列物质能共存于同一溶液中的是()。
A.NaCl,MgCl2
B.BaCl2,H2SO4
C.Ca(OH)2,H3PO4
D.AgNO3,FeCl3
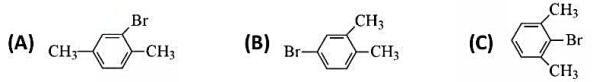
在下列各组化合物中,选择能满足各题具体要求者,并说明理由。
(1)下列哪一个化合物与KOH醇溶液反应,释放出F-?

(2)下列哪一个化合物在乙醇水溶液中放置,能形成酸性溶液?

(3)下列哪一个与KNH2在液氨中反应,生成两种产物?


 如果结果不匹配,请
如果结果不匹配,请 
















