 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在298K时,浓度为0.01mol·dm-3的HAc溶液在某电导池中测得电阻为2220Ω.已知该电导池常数 ,试求
在298K时,浓度为0.01mol·dm-3的HAc溶液在某电导池中测得电阻为2220Ω.已知该电导池常数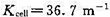 ,试求该条件下HAc的解离度和解离平衡常数。
,试求该条件下HAc的解离度和解离平衡常数。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在298K时,浓度为0.01mol·dm-3的HAc溶液在某电导池中测得电阻为2220Ω.已知该电导池常数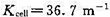 ,试求该条件下HAc的解离度和解离平衡常数。
,试求该条件下HAc的解离度和解离平衡常数。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在298K时,浓度为0.01mol·dm-3的HAc溶液在某…”相关的问题
更多“在298K时,浓度为0.01mol·dm-3的HAc溶液在某…”相关的问题
298K时,在Ag+/Ag电极中加入过量I-,设达到平衡时c(I-)=0.1mol·dm-3,而另一电极为Cu2+/Cu,c(Cu2+)=0.01mol·dm-3,将两电极组成原电池,写出原电池符号、电池反应,并求电池反应平衡常数。
已知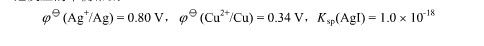
298K时,在某电导池内盛以浓度为 0.01mol·dm-3的KCI水溶液,测得电阻R为 484.0Ω。当盛以不同浓度的NaCl水溶液时测得数据如下

已知298 K时, 0.01 mol·dm-3的KCl水溶液的电导率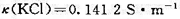 ,试求:
,试求:
(1)NaCl水溶液在不同浓度时的摩尔电导率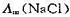 ;
;
(2)以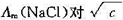 作图,求NaCl的无限稀释摩尔电导率
作图,求NaCl的无限稀释摩尔电导率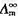 (NaCl)。
(NaCl)。
A.κ减小,Λm增加
B.κ增加,Λm减小
C.κ减小,Λm减小
D.κ增加,Λm增加
298K时,在0.01mol/kg的水杨酸(HA)溶液中含有0.01mol/kg的KCl和0.01mol/kg的Na2SO4。已知水杨酸在此温度下的Kc=1.06×10-5,求此混合溶液的离子强度。
在298K和标准压力时,电解一含Zn2+溶液,希望当Zn2+浓度降至1×10-4mol·kg-1时,仍不会有H2(g)析出,试问溶液的pH值应控制在多少为好?已知H2(g)在Zn(s)上的超电势为0.72V,并设此值与溶液浓度无关。
已知25℃时0.01mol·dm-3KCl溶液的电导率为0.141S·m-1,一电导池中充以此溶液,在25℃时测知其电阻为484Ω。在同一电导池中盛入同样体积的浓度分别为0.0005mol·dm-3、0.0010mol·dm-3、0.0020mol·dm-3和0.0050mol·dm-3的NaCl溶液,测出其电阻分别为10910、5494、2772和1128.9Ω。试用外推法求无限稀释时NaCl的摩尔电导率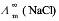 。
。
A.渗透浓度为40mmol·L-1NaCl
B.渗透浓度为10mmol·L-1Na3PO4
C.渗透浓度为400mmol·L-1Na3PO4
D.0.02mol·L-1Na2CO3
氯乙烯以AIBN为引发剂在50℃进行悬浮聚合,该温度下引发剂半衰期t1/2=74h,引发剂浓度为0.01mol·L-1,引发效率f=0.75,从理论上计算:(1)反应10h引发剂残留浓度;(2)初期生成聚氯乙烯的聚合度。试述从计算中受到什么启示。
某溶液中NaCl的浓度为0.001moL/kg,Na2SO4的浓度为0.003mol/kg,试计算298K时该溶液的(1)离子强度;(2)各离子的活度系数;(3)各化合物的离子平均活度。