 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知某反应的各物质浓度数据如下: aA(g) + bB(g) = 2C(g)起始浓度(mol·L-1) 3.01.002 s末浓度(mol·L-1) 1.80.60.8据此可推算出上述反应化学方程式中,各物质的化学计量数之比是()
A.9 : 3 : 4
B.3 : 1 : 2
C.2 : 1 : 3
D.3 : 2 : 1
 答案
答案
B、3 : 1 : 2
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.9 : 3 : 4
B.3 : 1 : 2
C.2 : 1 : 3
D.3 : 2 : 1
 答案
答案
B、3 : 1 : 2
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知某反应的各物质浓度数据如下: aA(g) + bB(g)…”相关的问题
更多“已知某反应的各物质浓度数据如下: aA(g) + bB(g)…”相关的问题
A.9∶3∶4
B.3∶1∶2
C.2∶1∶3
D.3∶2∶1
A.X2为0.2
B.Y2为0.2
C.Z为0.3
D.Z为0
A.0.2 mol•L-1•s-1
B.0.4 mol•L-1•s-1
C.0.6 mol•L-1•s-1
D.0.8 mol•L-1•s-1
A.平衡不移动
B.平衡向正反应方向移动
C.平衡向逆反应方向移动
D.正反应速率增大,逆反应速率减小
A.Z为0.3 mol•L-1
B.Y2为0.4 mol•L-1
C.X2为0.2 mol•L-1
D.Z为0.4 mol•L-1
A.容器内压强不随时间变化
B.容器内各物质的质量分数不随时间变化
C.容器内X、Y、Z的物质的量浓度之比是1:2:2
D.单位时间消耗0.1molX同时生成0.2mol Z
A.该反应为化合反应
B.待测值为18
C.反应中丁和丙的质量比为3:1
D.甲、丙两种物质化学计量数之比为1 : 2
化学反应如下:
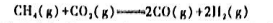
(1)利用教材附录中各物质的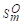 ,Δt
,Δt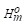 数据,求上述反应在25℃时的
数据,求上述反应在25℃时的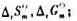
(2)利用教材附录中各物质的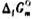 数据,计算上述及应在25℃时的
数据,计算上述及应在25℃时的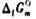 ;
;
(3)25℃,若始态CH4(g)和H2(g)的分压均为150kPa,末态CO(g)和H2(g)的分压均为50kPa,求反应的ΔtSm,ΔtGm.
粉煤灰是一种火山灰质材料,来源于煤中的无机组成,从粉煤灰中能够获得Al2O3,已知某火力发电厂的粉煤灰中的化学成分如下表。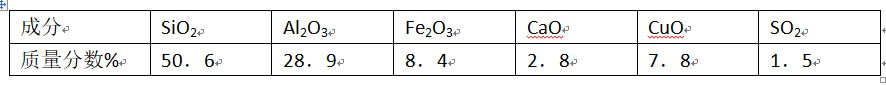 问题一、上述氧化物中能与水反应的是()。
问题一、上述氧化物中能与水反应的是()。
问题二、从粉煤灰中提取Al¬2O3的一种工艺流程如下:
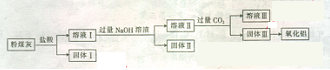
①体I中含有的主要物质的化学式为()。
②溶液Ⅱ中通人过量的CO2,发生反应的离子方程式为()。
问题三、氧化铝和焦炭的混合物与氮气在高温下反应,可制得新型非金属材料A1N与一种中学常见气体x。已知每转移3mol-,就有1.5mol化合物X生成,此反应的化学方程式为()。
A.物质的量浓度相同时,各溶液的pH关系为pH(Na2Y)>pH(NaX)>pH(NaHY)
B.mol·L-1HX溶液与bmol·L-1NaOH溶液等体积混合,所得溶液中存在c(Na+)>c(X-),则不一定a<b
C.在HX溶液中滴入Na2Y溶液,反应2HX+Y2-===2X-+H2Y成立
D.若0.1mol·L-1NaHY溶液呈酸性,则其水解能力小于电离能力
工业上以氨气为原料制备硝酸的过程如下: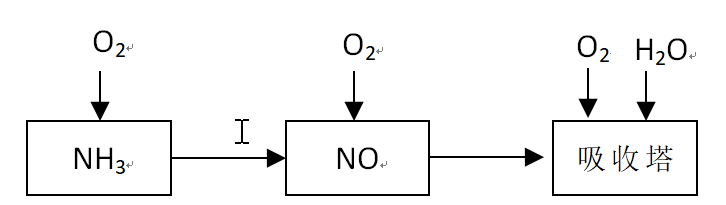 某课外小组模拟上述部分过程设计了如下实验装置制备硝酸(所有橡胶制品均已被保护)。
某课外小组模拟上述部分过程设计了如下实验装置制备硝酸(所有橡胶制品均已被保护)。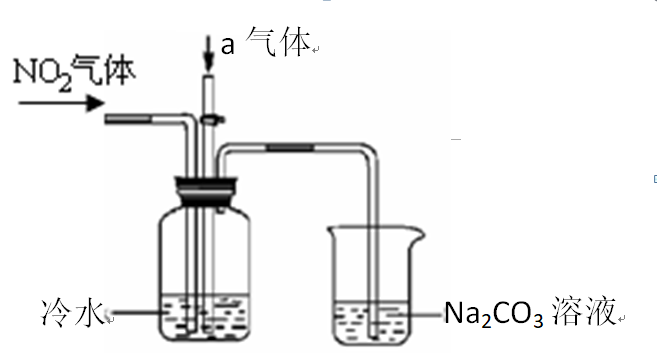
问题一、工业上用氨气制取NO的化学方程式是()。
问题二、连接好该装置后,首先进行的操作是()。
问题三、通入a气体的目的是()。
问题四、盛有Na2CO3溶液的烧杯为尾气处理装置,该装置中反应的化学反应方程式是2NO2+Na2CO3==NaNO2+()+()
问题五、已知:温度低于21.15℃时,NO2几乎全部转变为N2O4.工业上可用N2O4与水反应来提高硝酸产率。N2O4与a气体在冷水中生成硝酸的化学方程式是()。
问题六、一定条件下,某密闭容器中N2O4和NO2的混合气体到达平衡时,c(NO2)=0.50mol/L、c(N2O4)=0.125mol/L。则2NO2(g) N2O4(g)的平衡常数K=()。假设NO2起始浓度为2mol/L,相同条件下,NO2的最大转化率为()。
N2O4(g)的平衡常数K=()。假设NO2起始浓度为2mol/L,相同条件下,NO2的最大转化率为()。