 更多“一般取晶胞来研究金属的晶体结构。()”相关的问题
更多“一般取晶胞来研究金属的晶体结构。()”相关的问题
根据金属镁的晶体结构:
(1)画出金属镁晶体的六方晶胞沿c轴的投影图,标明各个原子的分数坐标及其在晶胞中摊到的个数;
(2)标明在晶胞内两个三角形中心处[坐标分别为(2/3,1/3)和(1/3,2/3)处]对称轴沿c轴的投影图;
(3)画出点阵单位沿c轴的投影,标明点阵单位内两个三角形中心处对称轴沿c轴的投影图,说明原子分数坐标、螺旋轴63和六次反轴6的定义。
已知NaCl的晶体结构如图C.17.1所示,它属于立方晶系,Oh点群。晶胞参数=564.0pm。
(I)写出通过晶胞中心的点对称元素。
(2)根据Na+和Cl-的离子半径值,了解在这结构中负离子是否接触?这种结构的稳定性如何?
(3)试计算NaCl晶体的密度D。
(4)将图C.17.1晶胞中顶角上的Na+和中心的Cl-除去,将Na+换成Nb2+,Cl-换得O2-即得NbO晶胞,试画出NbO的晶胞和其中原子簇的结构;已知晶跑参数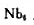 =421pm,计算晶体的密度i写出通过晶胞中心点的点对称元素和点群(Nb的相对原子质量为92.91);计算Nb2+的离子半径。
=421pm,计算晶体的密度i写出通过晶胞中心点的点对称元素和点群(Nb的相对原子质量为92.91);计算Nb2+的离子半径。
(5)将图C.17.1晶胞中面心和体心的原子除去,顶角上的Na+换成U6+,棱上的Cl-换成O2-,得UO3的晶体结构,立方晶胞参数a=415.6pm。试画出UO3晶胞的结构;写出通过晶胞中心点的点对称元素和点群;计算晶体的密度,计算U6+的离子半径(U的相对原子质量为238.0);画出由处在12条棱上的02-组成的立方八面体的图形;计算该多面体的自由孔径。
(1)画出C60的ccp结构沿四重轴方向的投影图;并用分数坐标示出分子间多面体空隙中心的位置(每类多面体空隙中心只写一组坐标即可)。
(2)在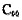 的ccp和hcp结构中,各种多面体空隙理论上所能容纳的“小球"的最大半径是多少?
的ccp和hcp结构中,各种多面体空隙理论上所能容纳的“小球"的最大半径是多少?
(3)C60分子还可形成非最密堆积结构,使某些碱金属离子填入多面体空隙,从而制得超导材料。在K3C60所形成的立方面心晶胞中,K+占据什么多面体空隙?占据空隙的百分数为多少?
A.对于一般结构构件取为1h
B.对于一般结构构件取为2h
C.对新型结构和跨度较大的试件取为12h
D.对新型结构和跨度较大的试件取为15h
一般灵敏度的确认,要根据()对允许金属通过大小来决定,其范围在0—99选择不正确的。
A.民航公安机关
B.民航总局
C.机场分局
D.维修部门
A.发散思维
B.聚集思维
C.结合思维
D.辐合思维
A.投资前准备主要包括:投资机会研究、可行性研究、投资决策三阶段
B.一般不允许同一家公司既承担可行性研究又承包建设
C.项目的实施通常包括四个阶段
D.咨询设计阶段,选择咨询设计公司应以其报价及公司财务状况来决定取舍
A.确定是否使用了一种金属合金来制作吉他的琴弦。
B.确定古典吉他演奏家使他们的琴弦死掉的速度是否比通俗吉他演奏家快。
C.确定把标准相同、长度相等的琴弦安在不同品牌的吉他上,是否以不同的速度死掉。
D.确定在新吉他弦上抹上不同的物质是否能使它们死掉。


 如果结果不匹配,请
如果结果不匹配,请 
















