 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
将反应设计成原电池.已知25°C;时, =-127.07kJ.mol-1.=-109.79kJ.mol-1,标准电极
将反应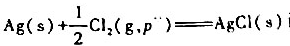 设计成原电池.已知25°C;时,
设计成原电池.已知25°C;时,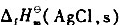 =-127.07kJ.mol-1.
=-127.07kJ.mol-1.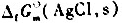 =-109.79kJ.mol-1,标准电极电势
=-109.79kJ.mol-1,标准电极电势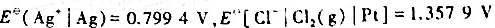 .
.
(1)写出电极反应和电池图示;
(2)求25°C、电池可逆放电2F电荷悬时的热Qz;
(3)求25°C时AgCl的活度积Kap.
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
将反应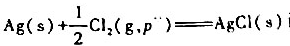 设计成原电池.已知25°C;时,
设计成原电池.已知25°C;时,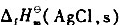 =-127.07kJ.mol-1.
=-127.07kJ.mol-1.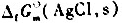 =-109.79kJ.mol-1,标准电极电势
=-109.79kJ.mol-1,标准电极电势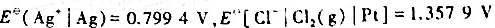 .
.
(1)写出电极反应和电池图示;
(2)求25°C、电池可逆放电2F电荷悬时的热Qz;
(3)求25°C时AgCl的活度积Kap.
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“将反应设计成原电池.已知25°C;时, =-127.07kJ…”相关的问题
更多“将反应设计成原电池.已知25°C;时, =-127.07kJ…”相关的问题
已知下列原电池:
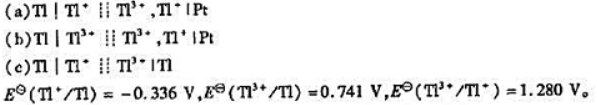
(1)写出各电池反应,并分别指出反应方程式中转移的电子数z;
(2)计算各电池的标准电动势EθMP;
(3)计算各电池反应的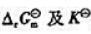 .
.
已知25℃甲酸甲酯的标准摩尔燃烧焓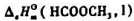 为-979.5kJ·mol-1,甲酸(HCOOH,I)、甲醇(CH3OH,1)、水(H2O,I)及二氧化碳(CO2,g)的标准摩尔生成焓
为-979.5kJ·mol-1,甲酸(HCOOH,I)、甲醇(CH3OH,1)、水(H2O,I)及二氧化碳(CO2,g)的标准摩尔生成焓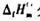 分别为-424.72kJ·mol-1,-238.66kJ·mol-1,-285.83kJ·mol-1及-393.509kJ·mol-1.应用这些数据求25℃时下列反应的标准摩尔反应焓.
分别为-424.72kJ·mol-1,-238.66kJ·mol-1,-285.83kJ·mol-1及-393.509kJ·mol-1.应用这些数据求25℃时下列反应的标准摩尔反应焓.

水的质子自递反应,已知在18℃时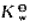 =6.4×10-15,25℃时
=6.4×10-15,25℃时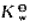 =1.0×10-14.
=1.0×10-14.
下列说法正确的是()。
A.水的质子自递反应是放热过程
B.水的质子自递反应是减反应
C.在18℃时,水的pH小于25℃时的pH
D.在18℃时,水中H+的浓度是8.0×10-8mol·L-1
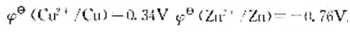 ,求此时原电池的电动势比标准状态时的电动势()
,求此时原电池的电动势比标准状态时的电动势()A.上升0.24V
B.下降0.24V
C.上升0.12V
D.下降0.12V
已知25℃时Hg(l)的摩尔体积Vm=1.482x10-5m3·mol-1,体膨胀系数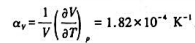 .恒温25℃时将1molHg(l)由100kPa加压到1100kPa,假设此过程Hg的体积变化可忽略不计,则过程的ΔS=()J·K-1.
.恒温25℃时将1molHg(l)由100kPa加压到1100kPa,假设此过程Hg的体积变化可忽略不计,则过程的ΔS=()J·K-1.
A.X>Y>Z
B.X>Z>Y
C.Z>X>Y
D.Z>Y>X
A.X>;Y>;Z
B.X>;Z>;Y
C.Z>;X>;Y
D.Z>;Y>;X
A.使用时间线
B.“鼠标经过图像”命令
C.将图形插入到表格中
D.使用AP Div元素与行为
(1)写出电池反应方程式;
(2)由附表六查得Eθ(Cl2/Cl-),计算E(Co2+/Co);
(3)p(Cl2)增大时,电池的电动势将如何变化?
(4)当CO2+浓度为0.010mol·L-1其他条件不变时,电池的电动势是多少伏?