 更多“氧在一些有机化合物中溶解度比水中为高。降低发酵液中水的极性可…”相关的问题
更多“氧在一些有机化合物中溶解度比水中为高。降低发酵液中水的极性可…”相关的问题
A.溶质和溶剂分子结构愈相似,溶质在溶剂中的溶解度越大
B.溶质本身的介电常数愈大,在介电常数愈大的溶剂中愈不易溶解
C.能和水分子形成氢键的化合物,比较容易溶解于水
D.邻苯二酚在水中的溶解度,大于间苯二酚和对苯二酚
A.Kow的数值越大,有机物在有机相中溶解度也越大
B.Kow反映了有机物的疏水性或脂溶性大小
C.Kow的数值越大,有机物在水中溶解度也越大
D.Kow越大,表明化合物越容易溶于非极性介质中,越容易被生物体细胞吸收
下列化合物中,在水中溶解度最小的是( )。
(A) NaF (B) KF (C) CaF2(D) BaF2
下列化合物中哪个在水中溶解度最大。()
A.CH3CH2CH2CH3;
B.CH3CH2OCH2CH3;
C.CH3CH2CH2CHO;
D.CH3CH2CH2CH2OH。
A.该物质有强氧化性主要原因是因为Z为最高正价
B.该化合物中所有元素的原子均达到8电子结构
C.X与Z的含氧酸均为强酸
D.X与Y的简单氢化物的熔沸点比Z的简单氢化物高,与氢键有关
A.氧化亚氮也叫一氧化二氮,俗称"笑气"。大气中的含量为310ppm,它能破坏臭氧层和增强温室效应。
B.氧化亚氮的沸点比氮、氧、氪、氙都高,随着液氧沸腾温度的升高,氧化亚氮在液氧中的溶解度增大。它在纯氧环境中,属易燃组分。
C.氧化亚氮在空分装置中的冻结,可使管道或换热器堵塞,还可引起主冷液氧中的碳氢化合物的局部积聚。
D.氧化亚氮在分子筛吸附器中能被部分吸附,一旦吸附剂表面的二氧化碳达到饱和,已吸附的氧化亚氮还会解吸出来随空气进入冷箱。
给出合理解释: (1)Ga的第一电离能(578.8kJ.mol-1)比Al的第一电离能(577.5kJ.mol-)要高。 (2)AlF3的熔点比AlCl3高得多。 (3)熔融的AlBr3不导电,而它的水溶液却是良导体。 (4)Tl(OH)与KOH的碱性一样。 (5)A1(Ⅲ)可以形成
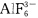 ,而B(Ⅲ)不能形成
,而B(Ⅲ)不能形成
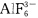 。 (6)能制得TlF3,但不能制得TlI3,却制得了TII。 (7)在蒸气下AlCl3为双聚体,而BCl3却不能发生二聚。 (8)TlI与KI同晶形,但TlI不溶于水。 (9)用路易斯酸碱理论和结构知识分析BF3和NH3作为酸碱的可能性。 (10)AlF3不溶于水,但可溶于HF中。 (11)BF3和BCl3中,哪一个是更好的电子接受体? (12)H3BO3在冷水中的溶解度很小,加热时,溶解度增大。 (13)BH3不存在,而BF3却能稳定存在。
。 (6)能制得TlF3,但不能制得TlI3,却制得了TII。 (7)在蒸气下AlCl3为双聚体,而BCl3却不能发生二聚。 (8)TlI与KI同晶形,但TlI不溶于水。 (9)用路易斯酸碱理论和结构知识分析BF3和NH3作为酸碱的可能性。 (10)AlF3不溶于水,但可溶于HF中。 (11)BF3和BCl3中,哪一个是更好的电子接受体? (12)H3BO3在冷水中的溶解度很小,加热时,溶解度增大。 (13)BH3不存在,而BF3却能稳定存在。


 如果结果不匹配,请
如果结果不匹配,请 
















