 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
当弱酸和弱酸盐组成的缓冲溶液组分浓度比为下述时,缓冲容量最大的是:()。
A.HA∶A—=1∶9
B.HA∶A—=9∶1
C.HA∶A—=2∶1
D.HA∶A—=1∶1
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.HA∶A—=1∶9
B.HA∶A—=9∶1
C.HA∶A—=2∶1
D.HA∶A—=1∶1
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“当弱酸和弱酸盐组成的缓冲溶液组分浓度比为下述时,缓冲容量最大…”相关的问题
更多“当弱酸和弱酸盐组成的缓冲溶液组分浓度比为下述时,缓冲容量最大…”相关的问题
称取仅含弱酸盐NaA和NaB的Na2CO3试样0.6125g,加水溶解后,以甲基橙为指示剂,用浓度为0.2000mol/L HCl标准溶液滴定,甲基橙变色时,消耗HCl标准溶液32.72mL;上述等量样品加水溶解后,若以酚酞为指示剂,用0.1000mol/L HCl标准溶液滴定,消耗25.34mL。(1)写出有关反应方程式;(2)各组分的质量分数是多少?(已知:弱酸HA的pKa=7.0,弱酸HB的pKa=1,MNa2CO3=105.99,MNaA=182.03,MNaB=132.0)
A.弱共辄酸碱对(包括弱酸―弱碱盐,弱碱―弱酸盐共辄酸碱对)
B.强共辄酸碱对(包括强酸-强碱盐,强碱-强酸盐共辄酸碱对)
C.弱共辄酸碱对(包括弱酸―弱酸盐,弱碱-弱碱盐共辄酸碱对)
D.强共辄酸碱对(包括强酸―强酸盐,强碱―强碱盐共辄酸碱对)
A.醋酸pKa=4、74
B.甲酸pKa=3、74
C.一氯乙酸pKa=2、86
D.二氯乙酸pKa=1、30
E.三氯乙酸pKa=、0、64
F.苯酚pKa=9、95
由一元弱酸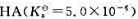 和它的共轭碱NaA组成的缓冲溶液中,HA的浓度为0.25mol·L-1.若在100mL此缓冲溶液中加入5.0mmolNaOH固体,溶液的pH变为5.60。计算加入NaOH固体前缓冲溶液的pH.
和它的共轭碱NaA组成的缓冲溶液中,HA的浓度为0.25mol·L-1.若在100mL此缓冲溶液中加入5.0mmolNaOH固体,溶液的pH变为5.60。计算加入NaOH固体前缓冲溶液的pH.
A.当总浓度一定时,缓冲比为1时β值最大
B.缓冲溶液稀释后缓冲比不变,所以pH不变,β也不变
C.缓冲溶液的有效缓冲范围为pKa±1
D.缓冲溶液的缓冲能力是在一定范围内的