 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
根据上题中所列化学反应方程式和条件,试计算发生下列变化时,△U与△H之间的能量差值。 (1) 2mol NH4HS(s)的分
根据上题中所列化学反应方程式和条件,试计算发生下列变化时,△U与△H之间的能量差值。
(1) 2mol NH4HS(s)的分解 (2) 生成1.00mol HCl(g)
(3) 5.00mol CO2(s)的升华 (4) 沉淀2.00mol AgCl(s)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
根据上题中所列化学反应方程式和条件,试计算发生下列变化时,△U与△H之间的能量差值。
(1) 2mol NH4HS(s)的分解 (2) 生成1.00mol HCl(g)
(3) 5.00mol CO2(s)的升华 (4) 沉淀2.00mol AgCl(s)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“根据上题中所列化学反应方程式和条件,试计算发生下列变化时,△…”相关的问题
更多“根据上题中所列化学反应方程式和条件,试计算发生下列变化时,△…”相关的问题
合成与制备:
(1)用化学反应方程式表示从海水提取溴的过程。
(2)用化学方法制备单质F,的步骤是
①在HF,KF存在下,用KMnO4氧化H2O2,制备K2MnF6;
②SbCl5和HF反应制备SbF5;
③K2MnF6和SbF5反应制得MnF4;
④不稳定的MnF4分解成MnF3和F2。
试写出以上各步的反应方程式。
(3)工业生产中以KCl为原料制备KClO和KClO3,试用化学反应方程式表示。
(4)以KBr为主要原料制备KBrO4,试用化学反应方程式表示。
(5)试说明实验室中制备SnCl4和AH3的方法,并写出化学反应方程式。
(6)试说明以TiO2和Cl2为主要原料制备TiCl4的具体方法,并写出化学反应方程式。
(7)工业上电解冷的NaCl稀溶液生产NaClO3试说明其过程并写出化学反应方程式。
某饱和土体,重度γ=19.5kN/m3,土粒比重ds=2.70,试求:
根据题中已知条件,推导干重度γd的表达式;
七种物质中的若干种。将此混合物加水后,可得白色沉淀和无色溶液。在此无色溶液中加入KSCN没有变化;无色溶液可使酸化后KMnO4溶液紫色褪去;将无色溶液加热有气体放出。另外,白色沉淀可溶于NH3·H2O中。试根据上述现象断:在混合物中哪些物质肯定存在,哪些肯定不存在,哪些可能存在。说明理由,并用化学反应方程式表示。
丙烷的燃烧反应方程式为
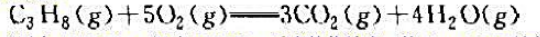
试计算在标准状态下(压力101325Pa、温度298K),反应的热效应(按1kmolC3H8计算).
①用铂丝蘸少量液体在火焰上灼烧,产生黄色火焰。
②它使酸化的KMnO4溶液褪色而产生无色溶液,此溶液与BaCl2溶液作用生成不溶于稀HNO3的白色沉淀。
③加入硫粉,并加热,硫溶解生成无色溶液,此溶液酸化时产生乳白色或浅黄色沉淀,此溶液也能使KI3溶液褪色,并能溶解AgBr。
推理判断:
(1)将白色固体化合物(A)加热,生成(B)和(C)。白色固体(B)可以溶于稀盐酸生成(D)的溶液,再向其中滴加适量氢氧化钠生成白色沉淀(E),氢氧化钠过量时沉淀消失。(C)是(F)的酸酐,浓酸(F)与单质硫作用生成有刺激性气味的气体化合物(G)和水,稀酸(F)与金属锌作用生成化合物(A)。
试给出(A),(B),(C),(D),(E),(F)和(G)的化学式,并完成各步的化学反应方程式。
(2)向化合物(A)的水溶液中,通入硫化氢气体,生成黑色沉淀(B),(B)经过过氧化氢处理转化成(C)。离心分离后将白色沉淀物(C)加热分解,得到(D)和(E)。(D)与氧化钡反应生成白色固体(F),(F)不溶于水,也不溶于稀硝酸。(E)与稀硝酸反应又生成(A)。(A)受热分解得黄色固体化合物(E),
试给出(A),(B),(C),(D),(E)和(F)的化学式,并完成各步的化学反应方程式。
(3)向化合物(A)的水溶液中,滴加一种钠盐(B)的溶液,先生成白色沉淀(C),(B)的溶液过量时沉淀消失生成(D),继续加入少许盐酸,产生有刺激性气味的气体(E)和黑色沉淀(F),同时体系呈乳白色浑浊状,表示有单质(G)生成。离心分离后固体物质(F)和(C)一同与过量稀硝酸共热,形成的溶液比(A)的溶液多出一种离子(H),因此可以与氯化钡反应生成白色沉淀(I);向清液中加入氯化钡溶液,亦有(I)生成,(I)不溶于稀硝酸。白色沉淀(C)不稳定,与水共存时有(F)和(H)生成。
试给出(A),(B),(C),(D),(E),(F),(G),(H)和(I)的化学式,并完成各步的化学反应方程式。
“设a1,a2,...,an是不同的整数,试证:当n>4时,(x-a1)(x-a2)...(x-an)+1是Q[x]中不可约多项式。”举例说明题中条件“n>4”不能去掉(除非n=1,3)。