 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
储有氧气的容器以速率。作直线运动,现使容器突然停止。(1)容器中氧气的温度将上升多少?(2)气体分子的平均平动动能和转动动能各增加多少? (以摩尔质量M和阿伏伽德罗常量NA表示。)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“储有氧气的容器以速率。作直线运动,现使容器突然停止。(1)容…”相关的问题
更多“储有氧气的容器以速率。作直线运动,现使容器突然停止。(1)容…”相关的问题
容积为0.5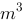 的刚性封闭容器储有0.65kg压力为120kPa的空气,将其加热到压力为150kPa,求传给空气的热量。空气
的刚性封闭容器储有0.65kg压力为120kPa的空气,将其加热到压力为150kPa,求传给空气的热量。空气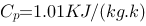 ,R=0.287
,R=0.287
A.40瓶
B.48瓶
C.50瓶
D.60瓶
A.7L
B.7.2L
C.8L
D.8.2L
一容器内储有氧气,其压强为1个大气压,温度为27℃,求:
(1)气体分子的数密度;
(2)气体的质量密度;
(4)分子间的平均距离;
(3)分子的平均动能.
(溶液混合问题)一容器内盛有50 L的盐水溶液,其中含有10 g的盐.现将每升含2 g盐的溶液以每分钟5 L的速率注入容器,并不断进行搅拌,使混合液迅速达到均匀,同时混合液以每分钟3 L的速率流出容器.问在任意时刻t容器中的含盐量是多少?
A.1-1/n
B.1/n-1
C.1n2-1
D.1-1/n2
A.将储存在气瓶内的高压气体减到所需要的压力
B.使工作压力自始至终保持稳定状态
C.当瓶中氧气压力达不到工作压力时可自动提高到所需工作压力
D.防止回火
过度排放CO2会造成”温室效应“,科学家正在研究如何将CO2转化为可以利用的资源,其中一种方案就是将CO2转化为可再生燃料甲醇(CH3OH)。其化学方程式为: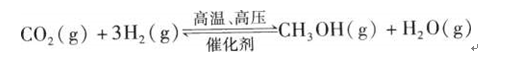
请填空:
问题一、写出上述反应的平衡常数表达式K=()。
问题二、在容积为2L的密闭容器中,用一定量二氧化碳与一定量氢气在一定条件下合成甲醇,实验结果如下图。以下说法正确的选项是()。
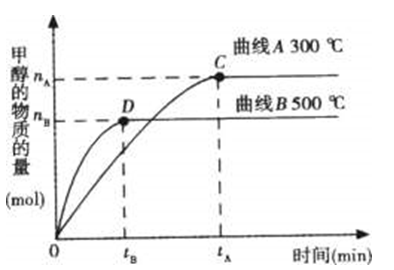
A在300℃,从反应开始到平衡,甲醇的平均反应速率
B反应体系从300℃升温到500℃,平衡常数K变大
C该反应的正反应为放热反应
D处于C点的反应体系从300℃升温到500℃n(H2)/n(CH3OH)增大
问题三、25℃、1.01×105Pa时16g液态甲醇完全燃烧,当恢复至原状态时,放出362.9kJ热量,此反应的热化学方程式为()。
问题四、选用合适的合金为电极,以氢氧化钠、甲醇、水、氧气为原料,可以制成一种以甲醇为原料的燃料电池,此燃料电池负极应加入或通入的物质是,正极的电极反应式为()。
A.4
B.3
C.2
D.1