 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
分析铁矿石中Fe的含量[以叫(Fe2O3)表示分析结果]测定4次,其结果分别为:67.48%、67.37%、67.43%、67.40%。求平均
分析铁矿石中Fe的含量[以叫(Fe2O3)表示分析结果]测定4次,其结果分别为:67.48%、67.37%、67.43%、67.40%。求平均偏差、标准偏差和相对标准偏差。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
分析铁矿石中Fe的含量[以叫(Fe2O3)表示分析结果]测定4次,其结果分别为:67.48%、67.37%、67.43%、67.40%。求平均偏差、标准偏差和相对标准偏差。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“分析铁矿石中Fe的含量[以叫(Fe2O3)表示分析结果]测定…”相关的问题
更多“分析铁矿石中Fe的含量[以叫(Fe2O3)表示分析结果]测定…”相关的问题
称取某铁矿石试样0.2500g。经一系列处理后,沉淀形式为Fe(OH)3称量形式为Fe2O3,称量质量为0.2490g,试求Fe和Fe3O4的质量分数。
准确称取铁矿石试样0.5000g,用酸溶解后加入SnCl2,使Fe3+还原为Fe2+,滴定Fe2+消耗24.50mLKMnO4标准溶液滴定,已知1mL.KMnO4相当于0.01260gH2C2O4·2H2O,(1)矿样中Fe及Fe2O3的质量分数各为多少?(2)取市售双氧水3.00mL,稀释定容于250.00mL,从中取出20.00mL试液,需用上述溶液KMnO421.18mL滴定至终点,计算每100.0mL市售双氧水所含H2O2的质量.
A.0.1g左右
B.0.2g左右
C.1g左右
D.0.35g左右
A.氯元素的化合价:―――――――→HCl Cl2 ClO2由低到高
B.溶于水后的溶液温度:―――――――――→NH4NO3 NaCl NaOH由高到低
C.地壳中元素含量:――――→O Fe Si由低到高
D.铁元素质量分数:――――――――→FeO Fe2O3 Fe3O4由低到高
称取2.200g KHC2O4·H2C2O4·2H2O配制于250mL容量瓶中,移取25.00mL,用NaOH滴定消耗24.00mL;移取25.00mL,于酸性介质中用KMnO4滴定消耗30.00mL,求此NaOH和KMnO4溶液的浓度。若用此KMnO4标准溶液测定样品中Fe含量,称取0.6000g样品消耗KMnO421.00mL,求算样品中Fe2O3的质量分数。
称取2.200g KHC2O4·H2C2O4·2H2O配制于250mL容量瓶中,移取25.00mL,用NaOH溶液滴定消耗24.00mL;移取25.00mL,于酸性介质中用KMnO4溶液滴定消耗30.00mL,求此NaOH和KMnO4溶液的浓度。若用此KMnO4标准溶液测定样品中的Fe含量,称取0.6000g样品,消耗KMnO4溶液21.00mL,求算样品中的Fe2O3%。
烧可得Fe2O3多少克?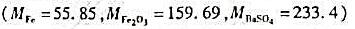
分析一磁铁矿0.5000g,得Fe2O3的质量为0.4980g。计算磁铁矿中铁及以Fe3O4计的含量。