 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
水中铁盐会导致红棕色Fe(OH)3在瓷水槽里沉积,通常用草酸(H2C2O4)溶液洗涤,以除去这种沉积物。试计算证明所列
水中铁盐会导致红棕色Fe(OH)3在瓷水槽里沉积,通常用草酸(H2C2O4)溶液洗涤,以除去这种沉积物。试计算证明所列两个方程中,哪一个更能表达Fe(OH)3的溶解原理。
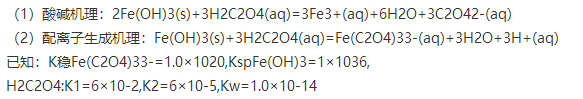
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
水中铁盐会导致红棕色Fe(OH)3在瓷水槽里沉积,通常用草酸(H2C2O4)溶液洗涤,以除去这种沉积物。试计算证明所列两个方程中,哪一个更能表达Fe(OH)3的溶解原理。
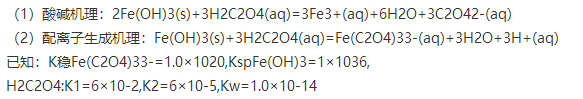
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“水中铁盐会导致红棕色Fe(OH)3在瓷水槽里沉积,通常用草酸…”相关的问题
更多“水中铁盐会导致红棕色Fe(OH)3在瓷水槽里沉积,通常用草酸…”相关的问题
A.上述反应中氧化剂和还原剂的物质的量之比为3:2
B.高铁酸钾中铁显+6价
C.由上述反应可知,Fe(OH)3的氧化性强于FeO42-
D.K2FeO4处理水时,不仅能消毒杀菌,而且生成的Fe3+水解形成Fe(OH)3胶体能吸附水中的悬浮杂质
A.MgCl2、CaCO3、Mg(OH)2
B.gCl、Ca(OH)2、Na2CO3
C.lCl3、Fe(OH)3、Ba(NO3)2
D.u(OH)2、ZnCO3、AgCl
饮用水中含有砷会导致砷中毒,水体中溶解的砷主要以As(Ⅲ)亚砷酸盐和As(Ⅴ)砷酸盐形式存在。
(1)33As与P位为同一主族,磷的原子结构示意图为(),砷在周期表中的位置()。
(2)根据元素周期律,下列说法正确的是()(填字母序号)。
a.酸性:H2SO4>H3PO4>H3AsO4
b.原子半径:S>P>As
C.非金属性:S>P>As
d.还原性:AsH3>PH3>H2S
(3)关于地下水中砷的来源有多种假设,其中一种认为是富含砷的黄铁矿(FeS2)被氧化为Fe(OH)3,同时生成SO42-,导致砷脱离矿体进入地下水FeS2被O2氧化的离子方程式为()。
(4)去除水体中的砷,可先将As(Ⅲ)转化为As(Ⅴ),选用NaClO可实现该转化.研究NaClO投加量对As(Ⅲ)氧化率的影响得到如下结果: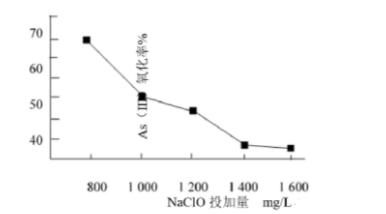 已知:投料前水样PH=5.81mol/LNaClO溶液PH=10.5,溶液中起氧化作用的物质是次氯酸,产生此结果的原因是()。
已知:投料前水样PH=5.81mol/LNaClO溶液PH=10.5,溶液中起氧化作用的物质是次氯酸,产生此结果的原因是()。
(5)强阴离子交换柱可以吸附以阴离子形态存在的As(Ⅴ)达到去除As的目的。已知:一定条件下,As(Ⅴ)的存在形式如下表所示: pH=6时,NaClO氧化亚砷酸(H3AsO3)的离子方程式是()。
pH=6时,NaClO氧化亚砷酸(H3AsO3)的离子方程式是()。
(1)属于微溶于水的是_________;水溶液能使酚酞试液变红的是___________________;
(2)不溶于水,但能溶于酸的是___________________________________;
(3)与酸反应溶液呈蓝色的是___________________________;
(4)水溶液通入CO2后有浑浊或沉淀出现的是______________。
A.Na2FeO4有强碱性,使细菌不能生存
B.Na2FeO4有强氧化性使细菌不能生存
C.Na2FeO4可水解生成Fe(OH)3胶体使水中的悬浮物凝聚沉降
D.Na2FeO4的还原产物可在水中生成Fe(OH)3胶体使水中的悬浮物凝聚沉降
A.3∶2
B.2∶3
C.8∶3
D.3∶8
A.3︰2
B.2︰3
C.8︰3
D.3︰8
A.硝酸电离出的H+,能被Zn、Fe等金属还原成H2
B.浓HNO3与浓HCl按3∶1的体积比所得的混合物叫王水
C.硝酸与金属反应时,主要是+5价的氮元素得电子
D.常温下,向浓HNO3中投入Fe片,会产生大量的红棕色气体
A.硝酸与金属反应时,主要是+5价的氮得电子
B.浓HNO3与浓HCl按3∶1的体积比所得的混合物叫王水
C.浓硝酸电离出的H+离子,能被Zn、Fe等金属还原成H2
D.常温下,向浓HNO3中投入Fe片,会产生大量的红棕色气体