 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在25℃时AgBr的溶度积常数为6.30×10-3。计算AgBr饱和溶液的电导率。
在25℃时AgBr的溶度积常数为6.30×10-3。计算AgBr饱和溶液的电导率。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在25℃时AgBr的溶度积常数为6.30×10-3。计算AgBr饱和溶液的电导率。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在25℃时AgBr的溶度积常数为6.30×10-3。计算Ag…”相关的问题
更多“在25℃时AgBr的溶度积常数为6.30×10-3。计算Ag…”相关的问题
已知25℃时AgBr的溶度积Ksp=4.88×10-13,EΘ(Ag+/Ag)=0.7994V,EΘ(Br2/Br-)=1.065V,试计算25℃时:(1)银-溴化银电极的标准电极电势EΘ(AgBr(s)/Ag);(2)AgBr(S)的标准生成吉布斯函数。
在25℃时测得碘酸铜饱和溶液的电导率为6.28×10-4S·cm-1,Cu2+和IO3-的摩尔电导率分别为55和41 S·cm2·mol-1。所用水的电导率小于1μs·cm-1,可以忽略不计。试求Cu(IO3)2的溶度积常数是多少?
下列电池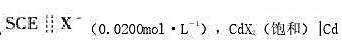 的电动势为-1.007V。计算CdX2的溶度积常数(不考虑液接电位,温度为25℃)。
的电动势为-1.007V。计算CdX2的溶度积常数(不考虑液接电位,温度为25℃)。
某学生为测定CuS的溶度积常数,设计如下原电池:正极为铜片,在0.1mol·dm-3Cu2+的溶液中,再通入H2S气体使之达到饱和;负极为标准锌电极。测得电池电动势为0.670V。已知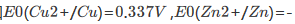 0.763V,H2S的
0.763V,H2S的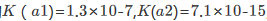 。试求CuS的溶度积常数。
。试求CuS的溶度积常数。
A.两种难溶强电解质相比较,标准溶度积常数较大的,其溶解度肯定也较大
B.将难溶强电解质的饱和溶液加水稀释时,难溶强电解质的标准溶度积常数不变,其溶解度也不变
C.难溶强电解质溶液的导电能力很弱,所以难溶强电解质均为弱电解质
D.难溶强电解质在水中达到溶解平衡时,电解质离子浓度的乘积就是该难溶强电解质的标准溶度积常数
的0.010mol·L-1AgNO3溶液与100.0mL的0,030mol·L-1NaIO3溶液混合,并稀释至500.0mL,然后过滤掉AgIO3沉淀.滤液的放射性计数为44.4s-1mL-1,原AgNO3溶液的放射性计数为74025s-1mL-1.计算KΘap(AgIO3).
已知25°C时水的离子积KW=1.008x10-14,NaOH,HCI和NaCl的Amm分别等于0.024811S.m2·mol-1.0.042616S.m2.mol-1和0.012645S.m2.mol-1.
(1)求25°C时纯水的电导率;
(2)利用上述纯水配制AgBr饱和水溶液,测得溶液的电导率k(溶液)=1.664x10-5S.m-1,求AgBr(s)在纯水中的溶解度.
已知25°C时AgBr的活度积Kap=4.88x10-13,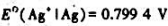 ,
,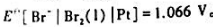 .试计算25℃时
.试计算25℃时
(1)银-溴化银电极的标准电极电势Eθ[Br-|AgBr(s)|Ag];
(2)AgBr(s)的标准摩尔生成吉布斯函数.
298K时,测得BaSO4饱和水溶液电导率为4.58×10-4S/m。已知该浓度时所用水的电导率为1.52×10-4S/m,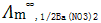 为1.351×10-2S·m2/mol,
为1.351×10-2S·m2/mol,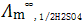 为4.295×10-2S·m2/mol,
为4.295×10-2S·m2/mol,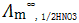 为4.211×10-2S·m2/mol。计算该温度下BaSO4的标准溶度积常数和溶解度。
为4.211×10-2S·m2/mol。计算该温度下BaSO4的标准溶度积常数和溶解度。