 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
溶液的pH=1,下列说法正确的是()
A.溶液显碱性
B.溶液中可以存在大量的OH-
C.溶液中一定存在有H+
D.溶液中可以存在大量的碳酸根离子
 答案
答案
C、溶液中一定存在有H+
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.溶液显碱性
B.溶液中可以存在大量的OH-
C.溶液中一定存在有H+
D.溶液中可以存在大量的碳酸根离子
 答案
答案
C、溶液中一定存在有H+
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“溶液的pH=1,下列说法正确的是()”相关的问题
更多“溶液的pH=1,下列说法正确的是()”相关的问题
A.厕所清洁剂加水稀释,溶液 pH 变小
B.厨房清洁剂可能含有 NaOH
C.两者混合使用能提高清洁效果
D.厕所清洁剂能使酚酞变色
A.中性溶液中一定是c(H+)=c(OH-)=1×10-7mol/L
B.向0.1mo1/L的盐酸溶液中加入适量的蒸馏水,则c(H+)、c(OH-)均减少
C.250C时,pH=9的溶液中不可能存在CH3COOH分子
D.250C时,pH=5的溶液中可能存在NH3·H2O分子
A.常温下pH=10的某碱溶液,取1 mL稀释到100 mL,稀释后pH为a,则a≥12
B.某温度下纯水中c(OH-)=2×10–7 mol·L-1,则该温度下0.1 mol·L–1的盐酸的pH=1
C.常温下pH=3的 H2SO4与pH=11的氨水等体积混合后,加入酚酞溶液仍为无色
D.用等浓度的NaOH溶液中和等体积pH=2与pH=3的醋酸,所消耗的NaO溶液的体积前者是后者的10倍
A.配制1 L 0.1 mol·L-1 NaCl溶液的实验中,用托盘天平称取5.85 g NaCl固体
B.用玻璃棒蘸取CH3COOH溶液点在用水润湿的pH试纸上测定该溶液的pH
C.用酸式滴定管量取25.00 mL高锰酸钾溶液
D.可用过滤的方法除去淀粉溶液中混有的少量NaCl杂质
A.标准状况下,44.8 L HF中含有氢原子的数目为2NA
B.8.0 g Cu2S和CuO的混合物中含有铜原子数为0.1NA
C.0.2 mol·L-1碳酸钠溶液中碳酸根的数目小于0.2NA
D.室温下,1 L pH=3的盐酸与1 L pH=3的CH3COOH溶液中,水电离出的H+数目均为10-3NA
A.(Na+)-c(X-)=9.9×10-7 mol•L-1
B.(Na+)=c(X-)+c(HX)=0.2 mol•L-1
C.(OH-)-c(HX)=c(H+)=1×10-6 mol•L-1
D.(Na+)>c(X-)>c(HX)>c(OH-)>c(H+)
A.厕所清洁剂加水稀释,溶液pH升高
B.厨房清洁剂应该含有碱性物质
C.两者混合使用能提高清洁效果
D.厕所清洁剂会腐蚀铁制下水道
A.滴定管用蒸馏水洗涤后,装入NaOH溶液进行滴定
B.随着NaOH溶液滴入,锥形瓶中溶液pH由小变大
C.用酚酞作指示剂,当锥形瓶中溶液由红色变无色时停止滴定
D.滴定达终点时,发现滴定管尖嘴部分有悬滴,则测定结果偏小
用NA代表阿伏加德罗常数的值,下列说法正确的是()。
A.
所含共价键数目均为0.4NA的白磷(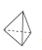 )和甲烷的物质的量相等
)和甲烷的物质的量相等
B.1molNa2O2与足量CO2充分反应转移的电子数目为2N
C.25℃时,pH=13的1.0LBa(OH)2溶液中含有的OH﹣数目为0.2NA
D.常温下,向1L0.1mol•L﹣1醋酸钠溶液中加入醋酸至中性,则溶液中CH3COO﹣的数目为0.1NA
A.厕所清洁剂加水稀释,溶液 pH 升高
B.厨房清洁剂可能含有 NaOH
C.混合使用能提高两者的清洁效果
D.厕所清洁剂可能使铁制下水道腐蚀
A.密闭容器中2 mol NO与1 mol O2充分反应,产物分子的数目为2NA
B.25℃,pH=13的NaOH溶液中含有OH-的数目为 0.1NA
C.标准状况下,22.4 L CCl4含CCl4分子数为NA
D.标准状况下,22.4L N2与CO混合气体的质量为28g