 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
()沉淀重量分析中沉淀反应是否完全的检验方法一般是
A.加入某中试剂观察
B.沉淀结晶大小
C.沉淀的溶解度大小
D.沉淀放置时间
 答案
答案
A、加入某中试剂观察
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.加入某中试剂观察
B.沉淀结晶大小
C.沉淀的溶解度大小
D.沉淀放置时间
 答案
答案
A、加入某中试剂观察
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“()沉淀重量分析中沉淀反应是否完全的检验方法一般是”相关的问题
更多“()沉淀重量分析中沉淀反应是否完全的检验方法一般是”相关的问题
问题1、向含铜粉的稀硫酸中滴加浓硝酸,写出该反应的离子方程式()。问题2、制备流程中的A操作名称是()。如果铜粉、硫酸及硝酸都比较纯净,则制得的CuSO4•5H2O中可能存在的杂质是(),除去这种杂质的实验操作称为()问题3、如果采用重量法测定CuSO4-5HO的含量,完成下列步骤。①()②加水溶解③加氯化钡溶液,沉淀④过滤(其余步骤省略)。在过滤前,需要检验是否沉淀完全,其操作是()。如果1.040g提纯后的试样中含CuSO•5HO的准确值为1.015g,而实验测定结果是1.000g,测定的相对误差为()问题4、已知:CuSO4+2NaOH→Cu(OH)2↓:1+Na2SO4.称取0.1000g某CuSO4•5H2O试样(杂质不与氢氧化钠溶液反应)于锥形瓶中,加入0.1000mo1/L氢氧化钠溶清28.00mL反府完全后,过量的氢氧化钠用0.1000mo1/L盐酸滴定至格点,托用盐酸20.16mL则0.1000g该试样中含CuSO4•5H2O()g上述滴定中,滴定管在用蒸馏水洗净之后,注入盐酸之前,还需进行的操作是()在滴定中,准确读数应该是滴定管上蓝线()所对应的刻度。
A.过量就行
B.按计量关系加入
C.过量20%~30%
D.过量50%~100%
E.沉淀剂达到近饱和
以粉煤灰(主要含Al2O3、SiO2,还有少量的Fe2O3)为原料制取Al2O3的流程如下: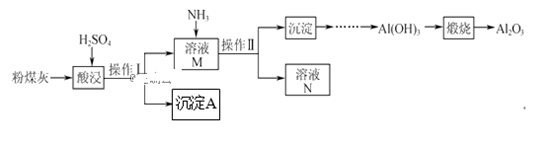 (1)操作Ⅰ的名称是()。
(1)操作Ⅰ的名称是()。
(2)用H2SO4“酸浸”时的离子方程式为()(任写一个)。
(3)简述如何检验酸浸后溶液中是否有Fe3+()。
(4)“煅烧”时的化学方程式为()。
(5)沉淀A与氢氟酸反应的化学方程式为()。
A.向某溶液中加入BaCl2溶液有白色沉淀出现,再加盐酸沉淀不消失,该溶液一定含SO42-
B.向某溶液中加入浓氢氧化钠溶液并加热,用湿润的蓝色石蕊试纸置于管口检验溶液中是否 存在NH4+
C.将某固体完全溶于盐酸,再滴加KSCN溶液,溶液未变红,该固体试样中也可能存在Fe3+
D.向无色溶液中加入盐酸,产生使澄清石灰水变浑浊的无色气体,该溶液中一定含有CO32-
A.加入NaOH溶液,有能使湿润的红色石蕊试纸变蓝的气体产生,说明一定含NH4+
B.先加入盐酸无现象,再滴加BaCl2 溶液产生白色沉淀,说明一定含有SO42-
C.先加入盐酸无现象,再滴加AgNO3 溶液产生白色沉淀,说明一定含有Cl-
D.蘸取溶液做焰色反应实验,火焰呈黄色,说明一定含有Na+一定不含K+
A.3
B.4
C.5
D.6
A.检验甲酸中是否混有甲醛,可先向样品中加入足量NaOH溶液中和甲酸,再进行银镜反应实验
B.检验纤维素水解产物时,应将脱脂棉与18.4mol/L的硫酸一起充分搅拌,然后加入新制Cu(OH)2并加热至沸腾,观察现象
C.用新制碱性氢氧化铜悬浊液鉴别乙醇、乙醛、乙酸三种物质的水溶液
D.通过向液态溴乙烷中滴加AgNO3溶液和稀HNO3观察有无淡黄色沉淀生成,以检验其中的溴元素
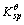 =1.2×10-10,SrCrO4的
=1.2×10-10,SrCrO4的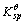 =2.2×10-5。
=2.2×10-5。
A.酯类在碱性条件下的水解反应叫做皂化反应
B.淀粉水解液加过量氢氧化钠溶液后,加银氨溶液并水浴加热可检测是否水解完全
C.纤维素在人体内可水解为葡萄糖,故可做人类的营养物质
D.饱和Na2SO4溶液或硫酸铜溶液均可使蛋白质溶液产生沉淀,但原理不同