 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
计算在标准状态下,氢分子的平均自由程和平均碰撞频率。 (取分子有效直径:2.7×10-10m;氢气的摩尔质量:2.02×1
计算在标准状态下,氢分子的平均自由程和平均碰撞频率。
(取分子有效直径:2.7×10-10m;氢气的摩尔质量:2.02×10-3kg/mol)
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
计算在标准状态下,氢分子的平均自由程和平均碰撞频率。
(取分子有效直径:2.7×10-10m;氢气的摩尔质量:2.02×10-3kg/mol)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“计算在标准状态下,氢分子的平均自由程和平均碰撞频率。 (取分…”相关的问题
更多“计算在标准状态下,氢分子的平均自由程和平均碰撞频率。 (取分…”相关的问题
氮分子的有效直径为3.8×10-10m,求它在标准状态下的平均自由程和连续两次碰撞间的平均时间间隔。
丙烷的燃烧反应方程式为
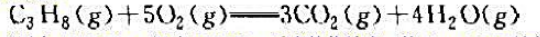
试计算在标准状态下(压力101325Pa、温度298K),反应的热效应(按1kmolC3H8计算).
在160km高空,空气密度为1.5×10-9kg/m3,温度为500K。分子直径以3.0×10-10m计,求该处空气分子的平均自由程与连续两次碰撞相隔的平均时间。
若某声波的波长等于标准状态下氧分子的平均自由程,已知氧分子的直径为3.00×10-10m,试问该声波的频率是多少?
标准状态下氦气(He)的粘度叩=1.89×10-5Pa·s,又Mmol=0.0040kg/mol,
设某理想气体A,其分子的最低能级是非简并的,取分子的基态作为能量零点,相邻能级的能量为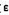 ,其简并度为2,忽略更高能级。(1)写出A分子的总配分函数的表达式;(2)设
,其简并度为2,忽略更高能级。(1)写出A分子的总配分函数的表达式;(2)设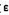 =kT,求出相邻两能级上最概然分子数之比N1/No的值;(3)设
=kT,求出相邻两能级上最概然分子数之比N1/No的值;(3)设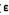 =kT,试计算在298K时,1molA分子气体的平均能量。
=kT,试计算在298K时,1molA分子气体的平均能量。