 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
根据德拜-休克尔极限定律,计算298K时0.005molkg的CaCl2水溶液中Ca2+和CI-的活度系数和离子平均活度系数。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“根据德拜-休克尔极限定律,计算298K时0.005molkg…”相关的问题
更多“根据德拜-休克尔极限定律,计算298K时0.005molkg…”相关的问题
2N2H4(l)+N2O4(g)=3N2(g)+4H2O(g)
根据教材附录中的数据。计算反应在298K时的标准摩尔焓变 。若反应的热能完全转化为势能, 可将100kg的重物垂直升高多少?已知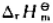 (N2H4,l)=50.63kJ·mol-1.
(N2H4,l)=50.63kJ·mol-1.
已知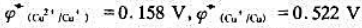 ,请计算反应2Cu+=Cu2++Cu在298K时的反应平衡常数.并由此说明+1价简单Cu+阳离子能否稳定存在于水溶液中?
,请计算反应2Cu+=Cu2++Cu在298K时的反应平衡常数.并由此说明+1价简单Cu+阳离子能否稳定存在于水溶液中?
298K时,在Fe3+,Fe2+的混合溶液中加入NaOH时,有Fe(OH)3和Fe(OH)2沉淀生成(假如没有其它反应发生)。当沉淀反应达到平衡时,保持c(OH-)=1.0molL-1,计算

已知电对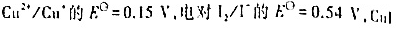 的
的
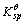 =1.3×10-12。
=1.3×10-12。
(1)试求氧化还原反应
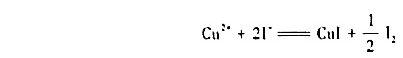
298K时的平衡常数;
(2)若溶液中Cu2+的起始浓度为0.10 mol·dm-3,I-的起始浓度为1.0 mol·dm-3,试计算达到平街时留在溶液中Cu2+的浓度。
(1)由附表六中查出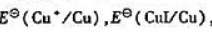 试计算
试计算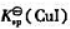 .
.
(2)计算298K下反应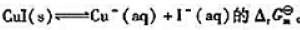
(3)若已知(2)中反应的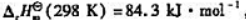 计算该反应的
计算该反应的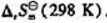
A.欧洲开始出现两大军事集团对峙局面
B.第一次世界大战的爆发
C.德意日三国法西斯军事同盟的形成
D.北约和华约组织的形成
A.反摩尔定律说,一个信息技术公司如果今天和18个月前卖掉同样多的同样产品,它的营业额就会降到一半。
B.安迪-比尔定律是约翰∙安迪与比尔∙盖茨共同提出。
C.贝佐斯定律是指在云的发展过程中,单位计算能力的价格大约每隔3年会降低50%。
D.当价格不变时,集成电路上可容纳的元器件的数目,约每隔18-24个月便会增加一倍,性能也按指数提升。