 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
问题1、1840年Devil用干燥的氧气通过干燥的硝酸银,得到N2O5,该反应的氧化产物是一种参与大气循环的气体,写出该反应的化学方程式()。问题2、F.Daniels等曾利用测压法在刚性反应器中研究了25℃时N2O5(g)分解反应2N205(g)→4NO2(g)+O2(g)+Q1(Q1<0),2NO2(g)
问题1、1840年Devil用干燥的氧气通过干燥的硝酸银,得到N2O5,该反应的氧化产物是一种参与大气循环的气体,写出该反应的化学方程式()。问题2、F.Daniels等曾利用测压法在刚性反应器中研究了25℃时N2O5(g)分解反应2N205(g)→4NO2(g)+O2(g)+Q1(Q1<0),2NO2(g) N204(g)+Q2(Q2>0)其中NO2二聚为N2O4的反应可以迅速达到平衡。体系的总压强P随时间t的变化如下表所示(t=00时,N2O5(g)完全分解);
N204(g)+Q2(Q2>0)其中NO2二聚为N2O4的反应可以迅速达到平衡。体系的总压强P随时间t的变化如下表所示(t=00时,N2O5(g)完全分解);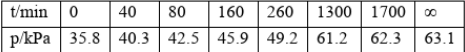 ①究表明,N2O5(g)分解的速率v=2x10-3Xpn2o5(kPa'min)。t=62min时,测得体系Po2=2.9kPa,则此时PN2O5:=()kPa,v=()(kPa/min)。②若提高反应温度至35℃,则N2O5(g)完全分解后体系压强P00(35℃)()63.1kPa(填“大于”、“等于”或“小于”),试从勒夏特列原理的角度加以解释()。③写岀N2O4(g)
①究表明,N2O5(g)分解的速率v=2x10-3Xpn2o5(kPa'min)。t=62min时,测得体系Po2=2.9kPa,则此时PN2O5:=()kPa,v=()(kPa/min)。②若提高反应温度至35℃,则N2O5(g)完全分解后体系压强P00(35℃)()63.1kPa(填“大于”、“等于”或“小于”),试从勒夏特列原理的角度加以解释()。③写岀N2O4(g) 2NO2(g)反应的平衡常数表达式()。问题3、对于反应2N2O5(g)→4NO2(g)+O2(g),R.A.Ogg提出如下反应历程:第一步:N2O5
2NO2(g)反应的平衡常数表达式()。问题3、对于反应2N2O5(g)→4NO2(g)+O2(g),R.A.Ogg提出如下反应历程:第一步:N2O5 NO2+NO3快速平衡第二步NO2+NO3→NO+NO2+O2慢反应第三步NO+NO3→2NO2快反应其中可近似认为第二步反应不影响第一步的平渐。下列表述错误的是()(填编号),A.v(第一步反应的逆反应)>v(第二步反应)B.反应的中间产物只有NO3C、该反应的速率主要由第二步决定D.N2O5的分解率主要由第一步决定
NO2+NO3快速平衡第二步NO2+NO3→NO+NO2+O2慢反应第三步NO+NO3→2NO2快反应其中可近似认为第二步反应不影响第一步的平渐。下列表述错误的是()(填编号),A.v(第一步反应的逆反应)>v(第二步反应)B.反应的中间产物只有NO3C、该反应的速率主要由第二步决定D.N2O5的分解率主要由第一步决定
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案


 更多“问题1、1840年Devil用干燥的氧气通过干燥的硝酸银,得…”相关的问题
更多“问题1、1840年Devil用干燥的氧气通过干燥的硝酸银,得…”相关的问题
















