 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
反应C(s)+H2O(g)-------- CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变会使反应速率加快的是()
A.增加 C的质量
B.将容器的体积缩小一半
C.保持体积不变,充入氦气使体系压强增大
D.保持压强不变,充入氮气使容器体积增大
 答案
答案
B、将容器的体积缩小一半
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.增加 C的质量
B.将容器的体积缩小一半
C.保持体积不变,充入氦气使体系压强增大
D.保持压强不变,充入氮气使容器体积增大
 答案
答案
B、将容器的体积缩小一半
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“反应C(s)+H2O(g)-------- CO(g)+H2…”相关的问题
更多“反应C(s)+H2O(g)-------- CO(g)+H2…”相关的问题
已知反应SnO2(s)+2H2(g)=Sn(s)+2H2O(g)和CO(g)+H2O(g)=CO2(g)+H2(g)的平衡常数分别为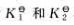 。则反应SnO2(s)+2CO(g)=2CO2(g)+Sn(s)
。则反应SnO2(s)+2CO(g)=2CO2(g)+Sn(s)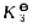 的=()。
的=()。
已知在298K时,下列反应:
①CO2(g)+2NH3(g)===H2O(g)+CO(NH2)2(s),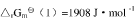
②
③C(石墨)+O2(g)===CO2(g),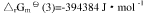
④N2(g)+3H2(g)===2NH3(g),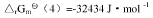 试求:(1)尿素CO(NH2)2(s)的标准摩尔生成Gibbs自由能
试求:(1)尿素CO(NH2)2(s)的标准摩尔生成Gibbs自由能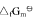 ;(2)由稳定单质生成尿素反应的平衡常数与上列反应平衡常数的关系式;(3)由单质生成尿素反应的平衡常数
;(2)由稳定单质生成尿素反应的平衡常数与上列反应平衡常数的关系式;(3)由单质生成尿素反应的平衡常数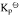 。
。
在一个抽空的容器中,放入过量的NH4HCO3(s)发生下列反应并达平衡:
NH4HCO3(s)====NH3(g)+H2O(g)+CO2(g)
系统的相数Ф=( );组分数K=( );自由度f=( )。
A.生成1molCO的同时生成1molH2
B.容器中物质的总质量不发生变化
C.n(H2O):n(H2)=1 :1
D.v逆(H2O)=v正(CO)
A.升高温度,可加快反应速率
B.将块状固体粉碎,可加快反应速率
C.平衡时,反应停止了
D.平衡时,CO的浓度不再改变
A.增加焦炭的量
B.保持体积不变,充入H2O气使体系的压强增大
C.将容器的体积增大一倍
D.将容器的体积缩小为一半
A.v(NH3)=0.01 mol·L−1·s−1
B.v(O2)=0.001 mol·L−1·s−1
C.v(NO)=0.001 mol·L−1·s−1
D.v(H2O)=0.045 mol·L−1·s−1
A.减小压强,平衡正向移动
B.加入固体碳,平衡正向移动
C.加入水蒸气,平衡不移动
D.升高温度,正反应速率增大,逆反应速率减小,平衡正向移动