 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
某基元反应:A→B其活化能Ea=60.4kg·mol-1,逆反应的活化能E'a=95.6kg·mol卐
某基元反应:A→B其活化能Ea=60.4kg·mol-1,逆反应的活化能E'a=95.6kg·mol-1,
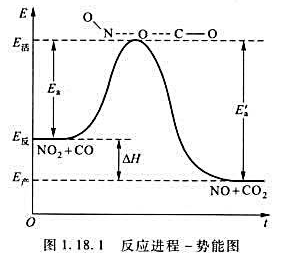
(1)试结合图1.18.1所示的反应进程-势能图,定性判断该反应是吸热反应,还是放热反应,求算该反应的ΔtH;
(2)若298K时的速率常数k=2.3×10-2s-1。试求373K时的速率常数;
(3)求算阿伦尼乌斯公式中的指前因子A。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案


 更多“某基元反应:A→B其活化能Ea=60.4kg·mol-1,逆…”相关的问题
更多“某基元反应:A→B其活化能Ea=60.4kg·mol-1,逆…”相关的问题
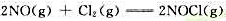 为基元反应。
为基元反应。















