 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知 298K,标准状态下求(3)CuO(s) = Cu(s)+1/2O2(g)的
已知 298K,标准状态下
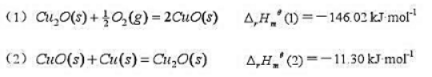
求(3)CuO(s) = Cu(s)+1/2O2(g)的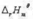
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知 298K,标准状态下
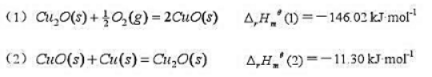
求(3)CuO(s) = Cu(s)+1/2O2(g)的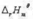
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知 298K,标准状态下求(3)CuO(s) = Cu(s…”相关的问题
更多“已知 298K,标准状态下求(3)CuO(s) = Cu(s…”相关的问题
丙烷的燃烧反应方程式为
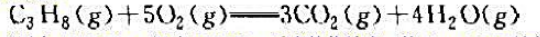
试计算在标准状态下(压力101325Pa、温度298K),反应的热效应(按1kmolC3H8计算).
已知298K时,Ca(OH)2(s)的 =-897.5kJ·mol-1,H2O(1)的
=-897.5kJ·mol-1,H2O(1)的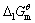 =-237.1kJ·mol-1,
=-237.1kJ·mol-1,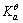 = 1.00×10-7,试求电对Ca(OH)2/Ca的电极电势。
= 1.00×10-7,试求电对Ca(OH)2/Ca的电极电势。
已知电对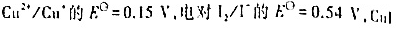 的
的
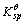 =1.3×10-12。
=1.3×10-12。
(1)试求氧化还原反应
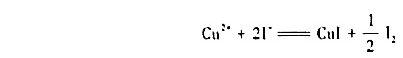
298K时的平衡常数;
(2)若溶液中Cu2+的起始浓度为0.10 mol·dm-3,I-的起始浓度为1.0 mol·dm-3,试计算达到平街时留在溶液中Cu2+的浓度。
(1)由附表六中查出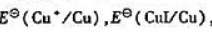 试计算
试计算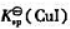 .
.
(2)计算298K下反应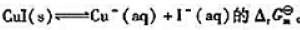
(3)若已知(2)中反应的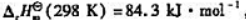 计算该反应的
计算该反应的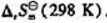
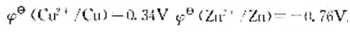 ,求此时原电池的电动势比标准状态时的电动势()
,求此时原电池的电动势比标准状态时的电动势()A.上升0.24V
B.下降0.24V
C.上升0.12V
D.下降0.12V
已知双曲线的中心在原点,焦点在x轴上,离心率等于3,并且经过点(-3,8)
求:(I)双曲线的标准方程;
(Ⅱ)双曲线的焦点坐标和准线方程。
将反应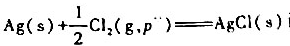 设计成原电池.已知25°C;时,
设计成原电池.已知25°C;时,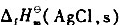 =-127.07kJ.mol-1.
=-127.07kJ.mol-1.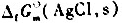 =-109.79kJ.mol-1,标准电极电势
=-109.79kJ.mol-1,标准电极电势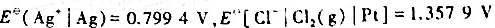 .
.
(1)写出电极反应和电池图示;
(2)求25°C、电池可逆放电2F电荷悬时的热Qz;
(3)求25°C时AgCl的活度积Kap.
已知25℃时,液态水的标准摩尔生成吉布斯函数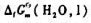 =-237.129kJ·mol-1,饱和蒸气压p''=3.1663kPa.求25℃时水蒸气的标准摩尔生成吉布斯函数.
=-237.129kJ·mol-1,饱和蒸气压p''=3.1663kPa.求25℃时水蒸气的标准摩尔生成吉布斯函数.
2N2H4(l)+N2O4(g)=3N2(g)+4H2O(g)
根据教材附录中的数据。计算反应在298K时的标准摩尔焓变 。若反应的热能完全转化为势能, 可将100kg的重物垂直升高多少?已知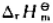 (N2H4,l)=50.63kJ·mol-1.
(N2H4,l)=50.63kJ·mol-1.