 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下列关于碱金属元素和卤素的说法错误的是()
A.随核电荷数的增加,碱金属元素和卤素的原子半径都逐渐增大
B.碱金属元素中,锂原子失去最外层电子的能力最弱;卤素中,氟原子得电子的能力最强
C.钾与水的反应比钠与水的反应更剧烈
D.碱金属元素的单质都可以保存在煤油中
 答案
答案
D、碱金属元素的单质都可以保存在煤油中
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.随核电荷数的增加,碱金属元素和卤素的原子半径都逐渐增大
B.碱金属元素中,锂原子失去最外层电子的能力最弱;卤素中,氟原子得电子的能力最强
C.钾与水的反应比钠与水的反应更剧烈
D.碱金属元素的单质都可以保存在煤油中
 答案
答案
D、碱金属元素的单质都可以保存在煤油中
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“下列关于碱金属元素和卤素的说法错误的是()”相关的问题
更多“下列关于碱金属元素和卤素的说法错误的是()”相关的问题
A.钾与水的反应比钠与水的反应更剧烈
B.溴单质与水的反应比氯单质与水的反应更剧烈
C.随核电荷数的增加,碱金属元素和卤素的原子半径都逐渐增大
D.碱金属元素中,锂原子失去最外层电子的能力最弱
海洋中蕴含丰富的资源,下图涉及多个以海水为原料的生产流程。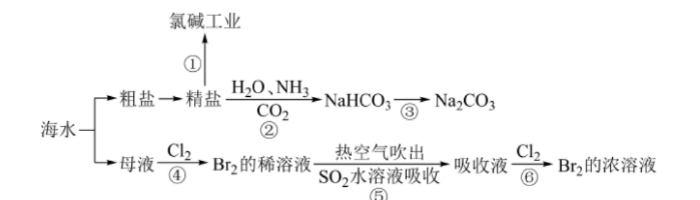 完成下列填空:
完成下列填空:
(1) 步骤①中电解饱和食盐水的化学方程式是()。
(2)工业上用Cl2与KOH(热溶液)制备KClO3,,Cl2+KOH=KCl+KClO3+H2O。配平上述反应方程式,并标出电子转移方向和数目()。
(3)关于卤素的下列说法错误的是()。
A、单质的熔点:Cl2>Br2>I2
B、元素的非金属性:Cl>Br>I
C、单质的氧化性:I2>Br2>Cl2
D、从海洋中获得Cl2,Br2的过程均涉及氧化还原反应
(4)对图中所示生产过程的说法正确的是()。
A、溶解度:NaHCO3>Na2CO3
B、第④⑤⑥步骤中,溴元素均被还原
C、第⑤⑥步骤的目的是进行溴的富集,提高Br2的浓度
D、联碱法与氨碱法相比,NaCl利用率较高,且能耗低
(5)步骤②是在饱和食盐水中先通入NH3再通入CO2,原因是()。
(6)某同学将CO2通入NaOH溶液中,当溶液呈中性时,溶液中浓度最大的微粒是()。
A、c(Na+)B、c(CO32-)C、c(HCO3-)D、c(H+)
A.卤素离子的还原性:F-<Cl-<Br-<I-
B.酸性:HIO4<HBrO4<HClO4
C.单质与氢气化合由难到易顺序:F2<Cl2<Br2<I2
D.氢卤酸的酸性:HF>HCl>HBr>HI
A.分子中官能团形成氢键的能力和官能团的离子化程度较大时,药物的水溶性增大
B.药物结构中含有卤素等原子时,药物的脂溶性增大
C.当药物分子中引入羧基时水溶性加大,此时脂水分配系数下降
D.药物结构中引入烃基时脂溶性增加,此时脂水分配系数降低
E.一般药物在脂溶性较低时,随着脂溶性增大,药物的吸收性提高
A.均为IA族元素,最外层均有一个电子
B.单质的还原性:Li>Na>K>Rb>Cs
C.碱性:LiOH<NaOH<KOH<RbOH<CsOH
D.从Li到Cs,核电荷数依次增加,电子层数、原子半径依次增大
A.谷氨酸是由5个碳原子、9个氢原子、1个氮原子和4个氧原子构成的
B.谷氨酸是由四种元素组成的
C.谷氨酸是有机物
D.谷氨酸中碳、氢原子个数比为5∶9
A.H原子得到一个电子实现最外电子层稳定结构
B.氢元素属于活泼非金属元素
C.与碱金属元素形成离子化合物:M+[∶H]-
D.H2中两个H原子间的化学键是共价键
A.在Spring配置文件中,可以通过<bean >元素的autowire属性指定自动装配方式
B.autowire属性值可以设置为none、byType、byName
C.autowire的属性值之一byType表示根据属性类型自动装配
D.通过<beans >元素的default-autowire属性,可以设置全局的自动装配方式