 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[多选题]
缓冲溶液的pH值决定于()。
A.此缓冲溶液的缓冲容量
B.组成此缓冲溶液弱酸或弱碱的Ka,Kb
C.共轭酸碱对的浓度比值的大小
D.此缓冲溶液的缓冲范围
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.此缓冲溶液的缓冲容量
B.组成此缓冲溶液弱酸或弱碱的Ka,Kb
C.共轭酸碱对的浓度比值的大小
D.此缓冲溶液的缓冲范围
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“缓冲溶液的pH值决定于()。”相关的问题
更多“缓冲溶液的pH值决定于()。”相关的问题
A.温度一定时,影响缓冲溶液pH值的主要因素为pKa和缓冲比
B.缓冲溶液的有效缓冲范围为pKa±1
C.缓冲溶液缓冲比一定时,总浓度越大,则其缓冲容量越大
D.缓冲溶液加水稀释后,pH值基本不变,缓冲容量也不变
A.缓冲溶液pH值的整数部分主要由pKa或pKb决定.其小数部分由
B.缓冲溶液的缓冲能力是无限的
C.或的值越大,缓冲能力越强
D.或的比值越小,缓冲能力越弱
A.当总浓度一定时,缓冲比为1时β值最大
B.缓冲溶液稀释后缓冲比不变,所以pH不变,β也不变
C.缓冲溶液的有效缓冲范围为pKa±1
D.缓冲溶液的缓冲能力是在一定范围内的
A.缓冲作用原理是因为溶液中含有足够浓度的共轭酸与共轭碱,通过质子转移平衡的移动,调节溶液的PH值不发生显著变化
B.缓冲溶液的PH值取决于共轭酸的离解常数与缓冲比
C.在缓冲比等于1时,缓冲溶液具有最大的缓冲容量
D.缓冲容量的大小与缓冲对的性质有关
由一元弱酸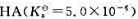 和它的共轭碱NaA组成的缓冲溶液中,HA的浓度为0.25mol·L-1.若在100mL此缓冲溶液中加入5.0mmolNaOH固体,溶液的pH变为5.60。计算加入NaOH固体前缓冲溶液的pH.
和它的共轭碱NaA组成的缓冲溶液中,HA的浓度为0.25mol·L-1.若在100mL此缓冲溶液中加入5.0mmolNaOH固体,溶液的pH变为5.60。计算加入NaOH固体前缓冲溶液的pH.
已知H2PO4的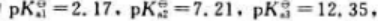
欲配制pH=3.00的缓冲溶液,应选择的缓冲对是().该缓冲溶液的缓冲范围是()。