 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知:2H2(g)+O2(g)=2H2O(l)△H=-571.6kJ·mol-1,CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890kJ·mol-1,现有H2与CH4的混合气体112L(标准状况),使其完全燃烧生成CO2和H2O(l),若实验测得反应放热3695kJ,则原混合气体中H2与CH4的物质的量之比是()。
A.1:1
B.1:3
C.1:4
D.2:3
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.1:1
B.1:3
C.1:4
D.2:3
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知:2H2(g)+O2(g)=2H2O(l)△H=-571…”相关的问题
更多“已知:2H2(g)+O2(g)=2H2O(l)△H=-571…”相关的问题
A.─ 484 kJ/mol
B.+ 484 kJ/mol
C.─ 242 kJ/mol
D.+ 242 kJ/mol
A.热化学方程式中化学计量数表示分子数
B.该反应ΔH2大于零
C.该反应ΔH2=-571.6 kJ·mol-1
D.该反应与上述反应属于可逆反应
已知下列化学反应的标准摩尔反应焓变,求乙炔(C2H2,g)的标准摩尔生成焓 。
。
(1)C2H2(g)+5/2O2(g)→2CO2(g)+H2O(g) =-1246.2kJ·mol-1
=-1246.2kJ·mol-1
(2)C(s)+2H2O(g)→CO2(g)+2H2(g) =+90.9kJ·mol-1
=+90.9kJ·mol-1
(3)2H2O(g)→2H2(g)+O2(g)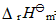 =+483.6kJ·mol-1
=+483.6kJ·mol-1
A.+478.7 kJ/mol
B.-764.5 kJ/mol
C.-478.7 kJ/mol
D.+764.5 kJ/mol
A.1∶1
B.1∶2
C.2∶3
D.3∶2
A.反应①中太阳能转化为化学能
B.反应②中电能转化为化学能
C.Q1>0、Q2<0
D.Q1=Q2
A.285.8kJ
B.-285.8kJ
C.571.6kJ
D.-571.6kJ
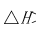 表明的是化合物H2O(g)的标准摩尔生成焓。( )
表明的是化合物H2O(g)的标准摩尔生成焓。( )A.2H2(g)+O2(g)→2H2O(g)
B.H2(g)+1/2O2(g)→H2O(g)
C.H2(g)+1/2O2(g)→H2O(l)
D.H2O(g)→H2(g)+1/2O2(g)
烟气的脱硫(除SO2)技术和脱硝(除NOx)技术都是环境科学研究的热点。
问题一、选择性催化复原法的脱硝原理为:

①上述反应中每转移3mol电子,生成标准状况下N2的体积为()L。
②已知:2H2(g)+O2(g)=2H2O(g)ΔH=-483.6kJ•mol-1
N2(g)+3H2(g)=2NH3(g)ΔH=-92.4kJ•mol-1
N2(g)+O2(g)=2NO(g)ΔH=-180.5kJ•mol-1
则反应6NO(g)+4NH3(g)=5N2(g)+6H2O(g)的ΔH=()。
问题二、目前,科学家正在研究一种以乙烯作为复原剂的脱硝(NO)原理,其脱硝机理示意图如以下图1,脱硝率与温度、负载率(分子筛中催化剂的质量分数)的关系如图2所示。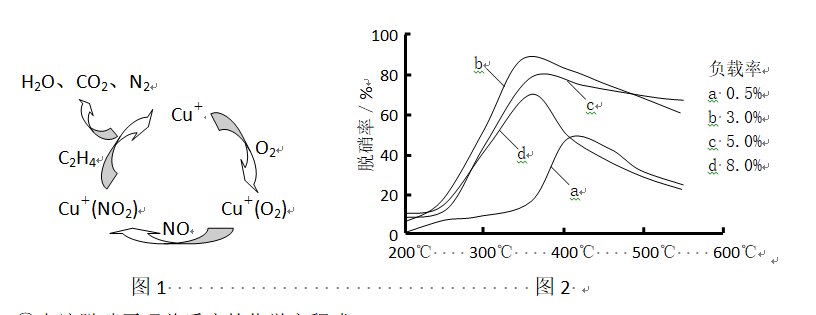
①出该脱硝原理总反应的化学方程式:()。
②为到达最正确脱硝效果,应采取的条件是()。
A.成键过程中吸收能量
B.断键过程中吸收能量,成键过程中释放能量
C.断键过程中释放能量
D.断键过程中释放能量,成键过程中吸收能量
已知反应SnO2(s)+2H2(g)=Sn(s)+2H2O(g)和CO(g)+H2O(g)=CO2(g)+H2(g)的平衡常数分别为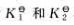 。则反应SnO2(s)+2CO(g)=2CO2(g)+Sn(s)
。则反应SnO2(s)+2CO(g)=2CO2(g)+Sn(s)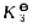 的=()。
的=()。