 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
称取某弱酸HA试样1.0264g,溶于适量水中,以酚酞为指示剂,用0.1000mol/LNaOH滴定,当滴定剂加到10.50mL时,溶液
称取某弱酸HA试样1.0264g,溶于适量水中,以酚酞为指示剂,用0.1000mol/LNaOH滴定,当滴定剂加到10.50mL时,溶液的pH为4.20;滴定至终点时,消耗NaOH溶液24.70mL。求:

 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
称取某弱酸HA试样1.0264g,溶于适量水中,以酚酞为指示剂,用0.1000mol/LNaOH滴定,当滴定剂加到10.50mL时,溶液的pH为4.20;滴定至终点时,消耗NaOH溶液24.70mL。求:

 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“称取某弱酸HA试样1.0264g,溶于适量水中,以酚酞为指示…”相关的问题
更多“称取某弱酸HA试样1.0264g,溶于适量水中,以酚酞为指示…”相关的问题
称取仅含弱酸盐NaA和NaB的Na2CO3试样0.6125g,加水溶解后,以甲基橙为指示剂,用浓度为0.2000mol/L HCl标准溶液滴定,甲基橙变色时,消耗HCl标准溶液32.72mL;上述等量样品加水溶解后,若以酚酞为指示剂,用0.1000mol/L HCl标准溶液滴定,消耗25.34mL。(1)写出有关反应方程式;(2)各组分的质量分数是多少?(已知:弱酸HA的pKa=7.0,弱酸HB的pKa=1,MNa2CO3=105.99,MNaA=182.03,MNaB=132.0)
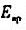 =0.82V。假设滴定过程中体积不变,求该有机酸的摩尔质量。
=0.82V。假设滴定过程中体积不变,求该有机酸的摩尔质量。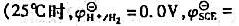
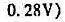
Na2S2O3溶液滴定.计算试样中KI的质量分数.
(已知CaO的摩尔质量58.06gmol1)
用KMnO4法测定硅酸盐样品中Ca2+的含量,称取试样0.5863g,在一定条件下,将钙沉淀为CaC2O4,过滤、洗涤沉淀,将洗净的CaC2O4溶于稀H2SO4中,用c(KMnO4)=0.05052mol/L的KMnO4标准滴定溶液滴定,消耗25.60mL,计算硅酸盐中Ca的质量分数。
A.由于硫酸密度较大,滴管从滴瓶拿出时,应将滴管横拿,避免溶液在转移至锥形瓶途中滴落损失
B.锥形瓶应先加入5omL蒸馏水,硫酸试样应沿锥形瓶下部内壁滴加,防止溶液溅出损失
C.滴加试样溶液同时应轻摇锥形瓶,使试样溶于水中
D.滴加试样速度防止过快,避免稀释时温度过高
准确量取30.00ml弱酸,加水稀释至100ml。以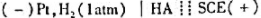 为测定电池,以0.1000mol/LNaOH溶液滴定弱酸HA。当酸被中和一半时,电池电动势为0.524V;化学计量点时,电池电动势为0.749V。φSCE=0.242V。计算:
为测定电池,以0.1000mol/LNaOH溶液滴定弱酸HA。当酸被中和一半时,电池电动势为0.524V;化学计量点时,电池电动势为0.749V。φSCE=0.242V。计算:
(1)弱酸HA的Ka。
(2)原弱酸HA的浓度。
已知某试样可能含有Na3PO4,Na3HPO4和惰性物质。称取该试样1.0000g,用水溶解。试样溶液以甲基橙作指示剂,用0.2500mol·L-1HCl溶液滴定,用去了32.00mL。含同样质量的试样溶液以百里酚酞作指示剂,需上述HCl溶液12.00mL。求试样中Na3PO4和Na2HPO4的质量分数。