 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知电子的成对能(P)与d轨道的分裂能(△o)的相对大小会影响八面体构型的配离子成为高自旋或低自旋的配离子。
已知电子的成对能(P)与d轨道的分裂能(△o)的相对大小会影响八面体构型的配离子成为高自旋或低自旋的配离子。下列论述正确的是
(A) P>△o)时形成低自旋配合物 (B) P<△o)时形成高自旋配合物
(C) P>△o)时形成高自旋配合物 (D) P<△o)时形成低自旋配合物
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知电子的成对能(P)与d轨道的分裂能(△o)的相对大小会影响八面体构型的配离子成为高自旋或低自旋的配离子。下列论述正确的是
(A) P>△o)时形成低自旋配合物 (B) P<△o)时形成高自旋配合物
(C) P>△o)时形成高自旋配合物 (D) P<△o)时形成低自旋配合物
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知电子的成对能(P)与d轨道的分裂能(△o)的相对大小会影…”相关的问题
更多“已知电子的成对能(P)与d轨道的分裂能(△o)的相对大小会影…”相关的问题
已知两个配离子的分裂能和成对能:
[Fe(CN)6]4-[Fe(H2O)6]2+
A/cm-133000 10400
P/cm-117600 17000

(2)写出A原子的电子排布式和元素符号();()。
(3)指出元素A在周期表中的位置()。
(4))指出元素A的最高化合价()。
(5)A的氢化物分子中共价键的类型可能有()。
①s-pσ键②p-pσ键③s-sσ键④p-pΠ键
(6)写出与A同周期未成对电子数最多的元素原子的价层电子排布式()。
X、Y、Z、R为前四周期原子序数依次增大的元素。X原子有3个能级,且每个能级上的电子数相等;Z原子的不成对电子数在同周期中最多,且Z的气态氢化物在同主族元素的氢化物中沸点最低;X、Y、R三元素在周期表中同族。
(1)R元素基态原子的价层电子排布式为()。
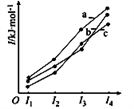
(2)下图表示X、Y、Z的四级电离能变化趋势,其中表示Y的曲线是()(填标号)。
 (3)化合物(XH2=X=O)分子中X原子杂化轨道类型分别是(),1mol(X2H5O)3Z=O分子中含有的σ键与π键的数目比为()。
(3)化合物(XH2=X=O)分子中X原子杂化轨道类型分别是(),1mol(X2H5O)3Z=O分子中含有的σ键与π键的数目比为()。
(4)Z与氯气反应可生成一种各原子均满足8电子稳定结构的化合物,其分子的空间构型为()。
(5)某R的氧化物立方晶胞结构如图所示,该物质的化学式为()。(用元素符号表示),已知该晶体密度为ρg/cm3,距离最近的原子间距离为dpm,则R的相对原子质量为()。(阿伏加德罗常数为NA)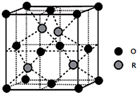
A.电子的动能变大,电势能变大,总能量变大
B.电子的动能变小,电势能变小,总能量变小
C.电子的动能变小,电势能变大,总能量不变
D.电子的动能变小,电势能变大,总能量变大
A.原子要吸收光子,电子的动能增大,原子的电势能增大,原子的能量增大
B.原子要放出光子,电子的动能减小,原子的电势能减小,原子的能量也减小
C.原子要吸收光子,电子的动能增大,原子的电势能减小,原子的能量增大
D.原子要吸收光子,电子的动能减小,原子的电势能增大,原子的能量增加
A.电子绕核运动有加速度,就要向外辐射电磁波
B.处于定态的原子,其电子做变速运动,但它并不向外辐射能量
C.原子内电子的可能轨道是不连续的
D.原子能级跃迁时,辐射或吸收光子的能量取决于两个轨道的能量差
A.原子核外电子排布式:M为1s22s2,N为1s2
B.结构示意图:M为 ,N为
C.M原子基态2p轨道上有一对成对电子,N原子基态3p轨道上有一对成对电子
D.M原子基态2p轨道上有1个未成对电子,N原子基态3p轨道上有1个未成对电子