 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
一种熔融碳酸盐燃料电池原理示意如图。下列有关该电池的说法正确的是()
A.电极A上H2和CO都发生了氧化反应
B.反应CH4+H2O=3H2+CO,每消耗1 mol CH4转移12 mol电子
C.电池工作时,电能转变为化学能
D.电极B上发生的电极反应为:O2+2H2O+4e−=4OH−
 答案
答案
A、电极A上H2和CO都发生了氧化反应
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.电极A上H2和CO都发生了氧化反应
B.反应CH4+H2O=3H2+CO,每消耗1 mol CH4转移12 mol电子
C.电池工作时,电能转变为化学能
D.电极B上发生的电极反应为:O2+2H2O+4e−=4OH−
 答案
答案
A、电极A上H2和CO都发生了氧化反应
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“一种熔融碳酸盐燃料电池原理示意如图。下列有关该电池的说法正确…”相关的问题
更多“一种熔融碳酸盐燃料电池原理示意如图。下列有关该电池的说法正确…”相关的问题
A.固体氧化物燃料电池
B.质子交换膜燃料电池
C.熔融盐燃料电池
D.碱性燃料电池
A.通CO的一极是电池的正极
B.负极发生的电极反应是O2+2CO2+4e-=2CO32-
C.负极发生的电极反应是CO+CO32--2e-=2CO2
D.正极发生氧化反应
A.气体R为NH3
B.(2)极的电极反应式为NO-3e-+4OH-===NO-3+2H2O
C.天然气碱性燃料电池的正极反应式为O2+4e-+2H2O===4OH-
D.每消耗8.4LCH4(标准状况)最多生成80gNH4NO3
A.电池工作时,COeq \o\al(2-,3)向负极移动
B.电池放电时,电子经外电路由通氧气的正极流向通氢气的负极
C.正极的电极反应为4OH--2e-===O2↑+2H2O
D.通氧气的电极为正极,发生氧化反应
KMnO4是一种重要消毒剂,俗名叫灰锰氧。
Ⅰ.某工厂以废旧锌锰电池为原料制备高锰酸钾的流程如下(部分产物已省略)
回答下列问题: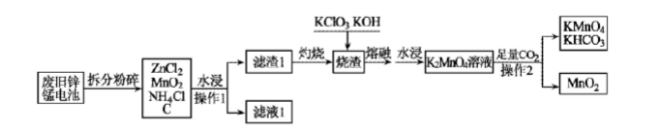 (1)K+的结构示意图为()。
(1)K+的结构示意图为()。
(2)这种锌锰电池放电时,负极的电极反应式为()。
(3)滤渣1“灼烧”的目的是();可循环利用的物质是()(填化学式)。
(4)“水浸”采用适当加热搅拌等措施,其目的是(),熔融“烧渣”可能产生的大气污染物是()。
(5)向K2MnO4溶液中通入足量CO2的离子方程式为:()。
Ⅱ.实验室中利用K2MnO4进行如下实验,下列说法错误的是()。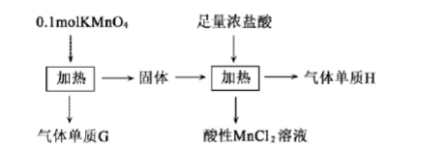 A、G与H均为氧化产物
A、G与H均为氧化产物
B、实验中KMnO4只作氧化剂
C、Mn元素至少参与了3个氧化还原反应
D、G与H的物质的量之和可能为0.25mol
A.2NaCl(熔融)===2Na+Cl2↑
B.MgO+H2===Mg+H2O
C.Fe3O4+4CO===3Fe+4CO2
D.2HgO===2Hg+O2↑
如图是2004年批量产生的笔记本电脑所用甲醇燃料电池的结构示意图。甲醇在催化剂作用下提供质子(H+)和电子,电子经外电路、质子经内电路到达另一极与氧气反应,电池总反应为:2CH3OH+3O2═2CO2+4H2O2。下列说法正确的是()。
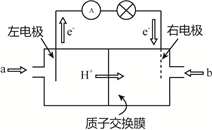
A.左电极为电池的正极,a处通入的物质是甲醇
B.右电极为电池的负极,b处通入的物质的空气
C.负极反应式为:CH3OH+H2O-6e-═CO2↑+6H+
D.正极反应式为:O2+2H2O+4e-═4OH-