 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
铝-空气燃料电池的电解液和反应()
A.以NaCl溶液或NaOH溶液为电解液时,正极反应都为:O22H2O4e=4OH
B.以NaOH溶液为电解液时,负极反应为:Al3OH3e=Al(OH)3↓
C.以NaOH溶液为电解液时,电池在工作过程中电解液的pH保持不变
D.电池工作时,电子通过外电路从正极流向负极
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.以NaCl溶液或NaOH溶液为电解液时,正极反应都为:O22H2O4e=4OH
B.以NaOH溶液为电解液时,负极反应为:Al3OH3e=Al(OH)3↓
C.以NaOH溶液为电解液时,电池在工作过程中电解液的pH保持不变
D.电池工作时,电子通过外电路从正极流向负极
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“铝-空气燃料电池的电解液和反应()”相关的问题
更多“铝-空气燃料电池的电解液和反应()”相关的问题
A.正极的电极反应为O2+2H2O+2e﹣=4OH﹣
B.负极的电极反应为Al+3OH﹣﹣﹣3e﹣═AI(OH)3↓
C.电池工作过程中,电解液的pH保持不变
D.电池使用时可能析出H2并放热
A.通入空气的一极为负极
B.H2、CO、CH4的混合气体在电池内部被氧化将化学能转化为电能
C.电池实际运行时的电解液应选择碱性溶液
D.电池的正极反应式为O2+4e-+2H2O===4OH-
A.以NaCl溶液或NaOH溶液为电解质溶液时,正极反应都为:O2+2H2O+4e-=4OH-
B.以NaOH溶液为电解质溶液时,负极反应为:Al+3OH--3e-= Al(OH)3↓
C.以NaOH溶液为电解质溶液时,电池在工作过程中电解质溶液的pH保持不变
D.电池工作时,电子通过外电路从正极流向负极
燃料电池是燃料的化学能不经过热机,而利用化学反应直接转化为电能的装置,图4-1所示是燃料电池一例.它的正电极及负电极被电解液分隔开(这与电解电池相似),现把氢气和氧气连续通入多孔Ni电极中,Ni电极浸在KOH电解液中,这时在两极将进行如下所示的化学反应:
正极:2H2+4OH-→4H2O+4e-;
负极:2H2O+4e-+O2→4OH-.
其总效果是

若燃料电池工作于298K定压下,△H=-571.6kJ·mol-1为反应前后焓的改变,两极电压为1.229V,试求这燃料电池的能源转换效率.

A.正极反应式为:O3+2H2O+4e-=4OH-
B.工作一段时间后,电解液中KOH的物质的量不变
C.该燃料电池的总反应方程式为:2H2+O2=2H2O
D.用该电池电解CuCl2溶液,产生2.24LCl2(标准状况)时,有0.1mol电子转移
A、氮气
B、氢气
C、氦气
D、二氧化碳
钛(Ti)被称为继铁、铝之后的第三金属,四川攀枝花和西昌地区的钒钛磁铁矿储量十分丰富。如以下图所示,将钛厂、氯碱厂和甲醇厂组成产业链可以大大提高资源利用率,减少环境污染。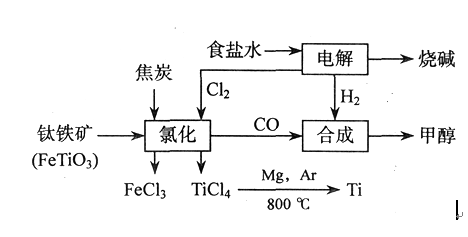 请填写以下空白:
请填写以下空白:
问题一、电解食盐水时,总反应的离子方程式是()。
问题二、写出钛铁矿经氯化法得到四氯化钛的化学方程式:()。
问题三、已知:①Mg(s)+Cl2(g)=MgCl2(s);△H=-641kJ/mol ②Ti(s)+2Cl2(g)=TiCl4(s);△H=-770kJ/mol。以下说法正确的选项是()。
AMg的燃烧热为641kJ/mol
BTi的能量一定比TiCl4高
C等质量的Mg(s)、Ti(s)与足量的氯气反应,前者放出的热量多
D该冶炼Ti法对环境友好
问题四、在上述产业链中,合成192t甲醇理论上需额外补充H2()t(不考虑生产过程中物质的任何损失)。
问题五、以甲醇、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池。该电池中负极上的电极反应式是()。
A.锌为正极,空气进入负极
B.负极反应为Zn → 2e— + Zn
C.电解液必定不是强酸
D.正极发生氧化反应2Zn → 2Zn2+ + 4e—
如图是2004年批量产生的笔记本电脑所用甲醇燃料电池的结构示意图。甲醇在催化剂作用下提供质子(H+)和电子,电子经外电路、质子经内电路到达另一极与氧气反应,电池总反应为:2CH3OH+3O2═2CO2+4H2O2。下列说法正确的是()。
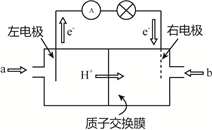
A.左电极为电池的正极,a处通入的物质是甲醇
B.右电极为电池的负极,b处通入的物质的空气
C.负极反应式为:CH3OH+H2O-6e-═CO2↑+6H+
D.正极反应式为:O2+2H2O+4e-═4OH-
近年来AIST报告正在研制一种“高容量、低成本”的锂—铜空气燃料电池。该电池通过一种复杂的铜腐蚀“现象”产生电力,其中放电过程为:2Li+Cu2O+H2O=2Cu+2Li++2OH一,下列说法不正确的是()。
A.放电时,Li+透过固体电解质向Cu极移
B.放电时,正极的电极反应式为O2+2H2O+4e一=4OH—
C.通空气时,铜被腐蚀,表面产生Cu2O
D.通空气时,整个反应过程中,铜相当于是催化剂