 更多“可溶性碳酸盐和碳酸氢盐溶于水时,溶液显示酸性。()”相关的问题
更多“可溶性碳酸盐和碳酸氢盐溶于水时,溶液显示酸性。()”相关的问题
溶液则转化为(D)并放出气体(E)。(A)的溶液与碘水作用则转化为(F),同时碘水褪色。(A)的溶液加入氯水则转化为溶液(G),(G)与钡盐作用,即产生不溶于强酸的白色沉淀(H)。(C)与溶液(D)混合后煮沸,则又缓慢转化为(A)。试给出(A),(B),(C),(D),(E),(F),(G)和(H)所代表的物质的化学式,并用化学反应方程式表示各过程。
A.水变成水蒸气时,化学性质发生了变化
B.碳在氧气中燃烧,它们的水分子都发生了变化
C.硫和碳放在一起时,它们的分子都发生了化学变化
D.盐溶于水时,盐分子和水分子都发生了化学变化
测得水层中含有0.233mmol的碘.计算碘在两分中的分配系数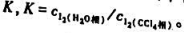 .设碘在两种溶剂中均以I2分子形式存在.
.设碘在两种溶剂中均以I2分子形式存在.
(2)若25℃I2在水中的浓度是1.33mmol.dm-3,求碘在CCl4中的浓度.
饲料级DL-蛋氨酸为()结晶,微溶于水,溶于稀盐酸及氢氧化钠溶液。无旋光性,有旋光性。
A.红棕色
B.粉红色
C.白色或淡灰色
D.黑色
A.具有还原性,易氧化
B.能和蛋白质或生物碱生成难溶于水的沉淀
C.能与三氯化铁反应呈蓝黑色或绿黑色,与铁氰化钾反应呈深红色
D.能与重金属盐如醋酸铅反应产生沉淀
E.易溶于极性溶剂
推理判断:
(1)将白色固体化合物(A)加热,生成(B)和(C)。白色固体(B)可以溶于稀盐酸生成(D)的溶液,再向其中滴加适量氢氧化钠生成白色沉淀(E),氢氧化钠过量时沉淀消失。(C)是(F)的酸酐,浓酸(F)与单质硫作用生成有刺激性气味的气体化合物(G)和水,稀酸(F)与金属锌作用生成化合物(A)。
试给出(A),(B),(C),(D),(E),(F)和(G)的化学式,并完成各步的化学反应方程式。
(2)向化合物(A)的水溶液中,通入硫化氢气体,生成黑色沉淀(B),(B)经过过氧化氢处理转化成(C)。离心分离后将白色沉淀物(C)加热分解,得到(D)和(E)。(D)与氧化钡反应生成白色固体(F),(F)不溶于水,也不溶于稀硝酸。(E)与稀硝酸反应又生成(A)。(A)受热分解得黄色固体化合物(E),
试给出(A),(B),(C),(D),(E)和(F)的化学式,并完成各步的化学反应方程式。
(3)向化合物(A)的水溶液中,滴加一种钠盐(B)的溶液,先生成白色沉淀(C),(B)的溶液过量时沉淀消失生成(D),继续加入少许盐酸,产生有刺激性气味的气体(E)和黑色沉淀(F),同时体系呈乳白色浑浊状,表示有单质(G)生成。离心分离后固体物质(F)和(C)一同与过量稀硝酸共热,形成的溶液比(A)的溶液多出一种离子(H),因此可以与氯化钡反应生成白色沉淀(I);向清液中加入氯化钡溶液,亦有(I)生成,(I)不溶于稀硝酸。白色沉淀(C)不稳定,与水共存时有(F)和(H)生成。
试给出(A),(B),(C),(D),(E),(F),(G),(H)和(I)的化学式,并完成各步的化学反应方程式。
A.盐化土
B.盐土
C.碱化土
D.碱土


 如果结果不匹配,请
如果结果不匹配,请 
















