 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下列离子方程式中书写正确的是()
A.铁和稀硫酸反应:2Fe+6H+===2Fe3++3H2↑
B.碳酸钙和稀盐酸反应:CaCO3+2H+===Ca2++CO2↑+H2O
C.盐酸除铁锈的反应:FeO+2H+===Fe2++H2O
D.硫酸镁溶液与氢氧化钡溶液反应:Mg2++2OH-===Mg(OH)2↓
 答案
答案
B、碳酸钙和稀盐酸反应:CaCO3+2H+===Ca2++CO2↑+H2O
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.铁和稀硫酸反应:2Fe+6H+===2Fe3++3H2↑
B.碳酸钙和稀盐酸反应:CaCO3+2H+===Ca2++CO2↑+H2O
C.盐酸除铁锈的反应:FeO+2H+===Fe2++H2O
D.硫酸镁溶液与氢氧化钡溶液反应:Mg2++2OH-===Mg(OH)2↓
 答案
答案
B、碳酸钙和稀盐酸反应:CaCO3+2H+===Ca2++CO2↑+H2O
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“下列离子方程式中书写正确的是()”相关的问题
更多“下列离子方程式中书写正确的是()”相关的问题
A.CO2通入NaAlO2溶液中AlO+CO2+H2O===Al(OH)3↓+CO
B.Al2O3与过量氨水Al2O3+6NH3•H2O===2Al3++6NH
C.向AlCl3溶液中加入过量NaOH溶液Al3++3OH-===Al(OH)3↓
D.向AlCl3溶液中滴入过量的氨水Al3++3NH3•H2O===Al(OH)3↓+3NH
A.铁与盐酸反响:2Fe+6H+=2Fe3++3H2↑
B.氯气与氯化亚铁溶液反响:2FeCl2+CI2=2FeCl3
C.氯化铁溶液与铁反响:Fe3++Fe=2Fe2+
D.氯化铁溶液与氢氧化钠溶液反响:Fe3++30H—=Fe(OH)3↓
以黄铁矿为原料制硫酸产生的废渣中含Fe2O3、SiO2、Al2O3、CaO、MgO等。现以此废渣制备铁红(Fe2O3)的过程如下。此浓度时,部分阳离子以氢氧化物形式沉淀时溶液的pH由见右表。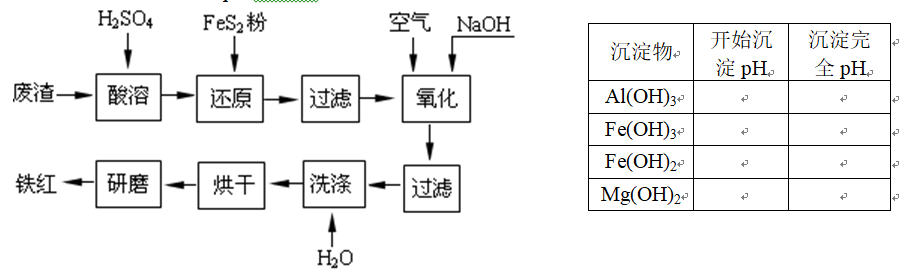 问题一、酸溶过程中Fe2O3与稀硫酸反应的化学方程式是()。
问题一、酸溶过程中Fe2O3与稀硫酸反应的化学方程式是()。
问题二、复原过程中加入FeS2是将溶液中的Fe3+复原为Fe2+,而本身被氧化为SO42-,写出有关的离子方程式:()。
问题三、氧化过程中通入空气和加入NaOH是为了将溶液中的铁元素充分转化为沉淀而析出,写出有关的离子方程式:()。
问题四、为了确保铁红的质量,氧化过程需要调节溶液pH的范围为()≤pH<()。
问题五、假设NaOH加入过量,所的铁红产品中有其它杂质,但可能无Al2O3,其原因是(用离子方程式表示):() 。
高铁酸钾是一种高效的多功能的水处理剂。工业上常采用NaClO氧化法生产,原理为:3NaClO+2Fe(NO3)3+10NaOH=2Na2FeO4↓+3NaCl+6NaNO3+5H2O Na2FeO4+2KOH=K2FeO4+2NaOH 主要的生产流程如下: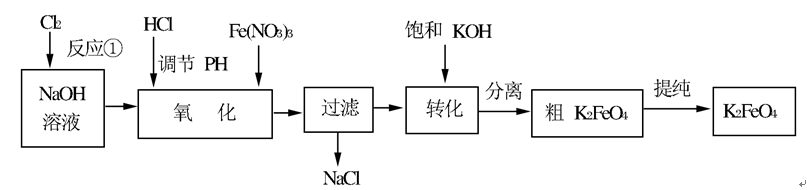 问题一、写出反应①的离子方程式()。
问题一、写出反应①的离子方程式()。
问题二、流程图中“转化”是在某低温下进行的,说明此温度下Ksp(K2FeO4)()Ksp(Na2FeO4)〔填“>”或“<”或“=”〕。
问题三、反应的温度、原料的浓度和配比对高铁酸钾的产率都有影响。
图1为不同的温度下,Fe(NO3)3不同质量浓度对生成率的影响;
图2为一定温度下,Fe(NO3)3质量浓度最正确时,NaClO浓度对K2FeO4生成率的影响
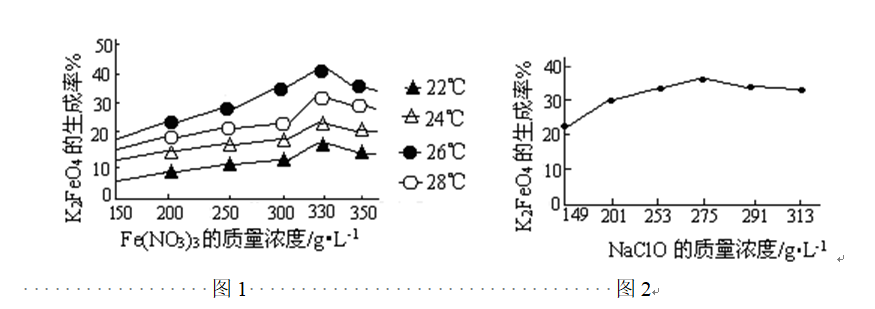
①工业生产中最正确温度为()℃,此时Fe(NO3)3与NaClO两种溶液最正确质量浓度之比为()。
②假设NaClO加入过量,氧化过程中会生成Fe(OH)3,写出该反应的离子方程式:()。假设Fe(NO3)3加入过量,在碱性介质中K2FeO4与Fe3+发生氧化复原反应生成K3FeO4,此反应的离子方程式:()。
问题四、K2FeO4在水溶液中易水解:
4FeO42—+10H2O 4Fe(OH)3+8OH—+3O2↑。在“提纯”K2FeO4中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用溶液()(填序号)。
4Fe(OH)3+8OH—+3O2↑。在“提纯”K2FeO4中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用溶液()(填序号)。
AH2O
BCH3COONa、异丙醇
CNH4Cl、异丙醇
DFe(NO3)3、异丙醇
A.次氯酸钙溶液中通入过量的二氧化碳Ca2++2ClO﹣+H2O+CO2═CaCO3↓+2HClO
B.硫酸亚铁溶液中加入过氧化氢溶液Fe2++2H2O2+4H+═Fe3++4H2O
C.用氨水吸收少量二氧化硫OH﹣+SO2═HSO3﹣
D.硝酸铁溶液加入过量氨水3NH3•H2O+Fe3+═Fe(OH)3↓+3NH4+
A.所有铵盐受热均可以分解,产物均有NH3
B.所有铵盐都易溶于水,所有铵盐中的N均呈-3价
C.NH4Cl溶液中加入NaOH浓溶液共热时反应的离子方程式为NH4++OH-=(加热)NH3↑+H2O
D.NH4Cl和NaCl的固体混合物可用升华法分离
高铁酸钾是一种高效的多功能水处理剂,具有氧化、吸附、絮凝、、助凝、杀菌、除臭等作用,高铁酸钾的开发和利用正日益显示出其广阔的应用前景。其制备路线如下: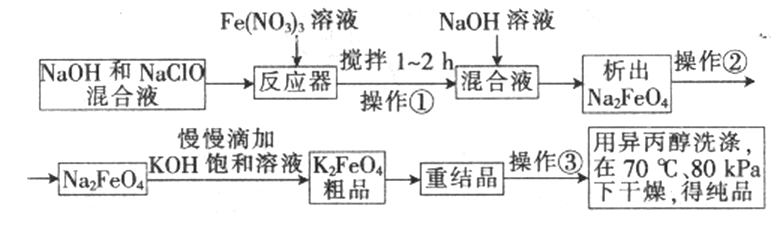
试答复以下问题:
问题一、操作①搅拌的目的是:()。
问题二、操作②与操作③相同,该操作名称是:()。
问题三、反应器中,NaOH、NaClO及Fe(NO3)3反应的离子方程式为:()。
问题四、次氯酸钠浓度对高铁酸钾产率有一定影响,当高铁酸钾产率最高时,NaClO的物质的量浓度约为()。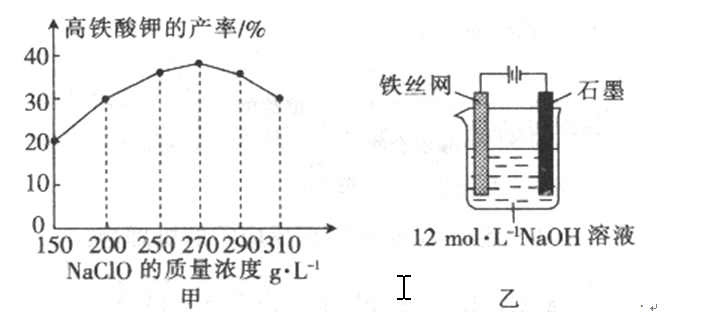
问题五、从环境保护的角度看,制备中间产物Na2FeO4较好的方法为电化学法,其装置如图乙所示,则阳极的电极反应式为()。
A.硝酸银与盐酸;硝酸银与氯化钠
B.盐酸与碳酸钙;盐酸与碳酸钠
C.氯化钡与硫酸钠;氢氧化钡与硫酸
D.氢氧化钾与硫酸镁;氢氧化钡与硫酸镁
A.Fe+S=FeS△H=-95.6kJ/mol(反应热)
B.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=+57.3kJ/mol(中和热)
C.C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(g)△H=-1367.0kJ/mol(燃烧热)
D.S(s)+O2(g)=SO2(g)△H=-269.8kJ/mol(反应热)