 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
Cu2S可与一定浓度的HNO3反应,生成Cu(NO3)2、CuSO4、NO2、NO和H2O,当NO2和NO的物质的量之比为1∶1时,实验参加反应的Cu2S和HNO3的物质的量之比为()。
A.1∶7
B.1∶9
C.1∶5
D.2∶9
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.1∶7
B.1∶9
C.1∶5
D.2∶9
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“Cu2S可与一定浓度的HNO3反应,生成Cu(NO3)2、C…”相关的问题
更多“Cu2S可与一定浓度的HNO3反应,生成Cu(NO3)2、C…”相关的问题
A.9.0L
B.13.5L
C.15.7L
D.16.8L
A.1∶1
B.5∶16
C.2∶3
D.3∶2
A.KNO3
B.K2CO3
C.K2SO4
D.KCl 使用与环保
A.容器中,SO2、O2与SO3共存且浓度相等
B.容器中,SO2、O2与SO3的物质的量之比为2︰1︰2
C.正反应生成SO3的速率等于逆反应生成O2的速率
D.反应容器内混合气体平均式量不随时间的变化而改变
A.①②④
B.②③
C.②④
D.①③④
A.5:3
B.5:4
C.1:1
D.3:5
A.反应过程中,被氧化与被还原的元素的物质的量之比为1:2
B.NF3是一种无色、无臭的气体,因此NF3在空气中泄漏时不易被察觉
C.若反应中转移的电子数目为6.02×1023,则可生成22.4L NO气体(标准状况)
D.一旦NF3泄漏,可以用石灰水溶液喷淋的方法减少污染
高铁酸钾是一种高效的多功能的水处理剂。工业上常采用NaClO氧化法生产,原理为:3NaClO+2Fe(NO3)3+10NaOH=2Na2FeO4↓+3NaCl+6NaNO3+5H2O Na2FeO4+2KOH=K2FeO4+2NaOH 主要的生产流程如下: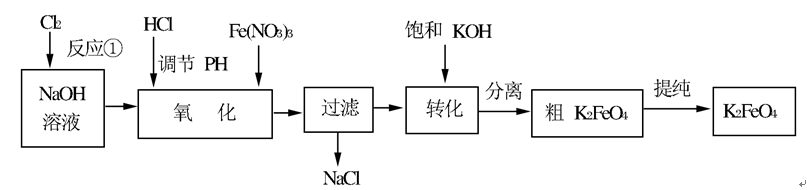 问题一、写出反应①的离子方程式()。
问题一、写出反应①的离子方程式()。
问题二、流程图中“转化”是在某低温下进行的,说明此温度下Ksp(K2FeO4)()Ksp(Na2FeO4)〔填“>”或“<”或“=”〕。
问题三、反应的温度、原料的浓度和配比对高铁酸钾的产率都有影响。
图1为不同的温度下,Fe(NO3)3不同质量浓度对生成率的影响;
图2为一定温度下,Fe(NO3)3质量浓度最正确时,NaClO浓度对K2FeO4生成率的影响
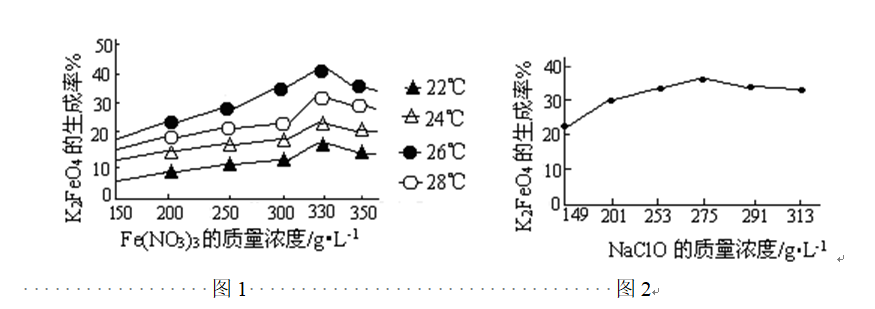
①工业生产中最正确温度为()℃,此时Fe(NO3)3与NaClO两种溶液最正确质量浓度之比为()。
②假设NaClO加入过量,氧化过程中会生成Fe(OH)3,写出该反应的离子方程式:()。假设Fe(NO3)3加入过量,在碱性介质中K2FeO4与Fe3+发生氧化复原反应生成K3FeO4,此反应的离子方程式:()。
问题四、K2FeO4在水溶液中易水解:
4FeO42—+10H2O 4Fe(OH)3+8OH—+3O2↑。在“提纯”K2FeO4中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用溶液()(填序号)。
4Fe(OH)3+8OH—+3O2↑。在“提纯”K2FeO4中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用溶液()(填序号)。
AH2O
BCH3COONa、异丙醇
CNH4Cl、异丙醇
DFe(NO3)3、异丙醇
A.氮气是由氮原子构成的双原子分子,所以化学性质不活泼
B.1mol可与3mol完全反应生成2mol
C.电闪雷鸣的雨天,雨水中会含有一定量的硝酸,其中发生的反应之一是
D.NO、在一定条件下可相互转化,且二者都是引起光化学烟雾的大气污染物
A.正常情况下,维生素D的合成与分泌是根据机体需要受血中25OHD的浓度自行调节
B.生成的1,25-(OH)2D的量达到一定水平时,可促进25-OHD在肝内的羟化、1,25-(OH)2D在肾脏羟化过程
C.肾脏生成1,25-(OH)2D间接受血钙浓度调节
D.血磷降低可直接促肾脏内25-OHD羟化生成1,25-(OH)2D的增加