 更多“铁生锈的过程,用方程式表达()。”相关的问题
更多“铁生锈的过程,用方程式表达()。”相关的问题
以黄铁矿为原料制硫酸产生的废渣中含Fe2O3、SiO2、Al2O3、CaO、MgO等。现以此废渣制备铁红(Fe2O3)的过程如下。此浓度时,部分阳离子以氢氧化物形式沉淀时溶液的pH由见右表。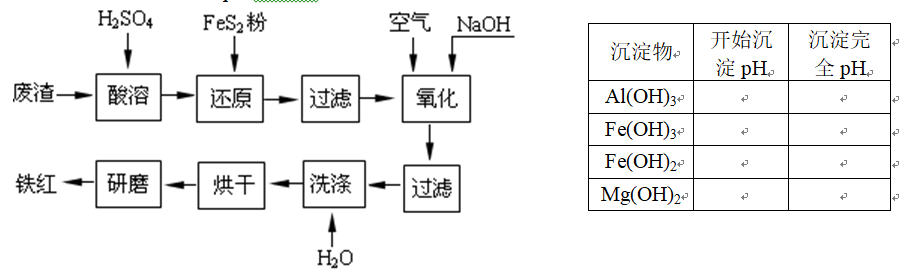 问题一、酸溶过程中Fe2O3与稀硫酸反应的化学方程式是()。
问题一、酸溶过程中Fe2O3与稀硫酸反应的化学方程式是()。
问题二、复原过程中加入FeS2是将溶液中的Fe3+复原为Fe2+,而本身被氧化为SO42-,写出有关的离子方程式:()。
问题三、氧化过程中通入空气和加入NaOH是为了将溶液中的铁元素充分转化为沉淀而析出,写出有关的离子方程式:()。
问题四、为了确保铁红的质量,氧化过程需要调节溶液pH的范围为()≤pH<()。
问题五、假设NaOH加入过量,所的铁红产品中有其它杂质,但可能无Al2O3,其原因是(用离子方程式表示):() 。
合成与制备:
(1)用化学反应方程式表示从海水提取溴的过程。
(2)用化学方法制备单质F,的步骤是
①在HF,KF存在下,用KMnO4氧化H2O2,制备K2MnF6;
②SbCl5和HF反应制备SbF5;
③K2MnF6和SbF5反应制得MnF4;
④不稳定的MnF4分解成MnF3和F2。
试写出以上各步的反应方程式。
(3)工业生产中以KCl为原料制备KClO和KClO3,试用化学反应方程式表示。
(4)以KBr为主要原料制备KBrO4,试用化学反应方程式表示。
(5)试说明实验室中制备SnCl4和AH3的方法,并写出化学反应方程式。
(6)试说明以TiO2和Cl2为主要原料制备TiCl4的具体方法,并写出化学反应方程式。
(7)工业上电解冷的NaCl稀溶液生产NaClO3试说明其过程并写出化学反应方程式。
某氮肥厂氨氮废水中的氮元素多以NH和NH3·H2O的形式存在,该废水的处理流程如下:![]()
问题一、过程Ⅰ:加NaOH溶液,调节pH至9后,升温至30℃,通空气将氨赶出并回收。
①用离子方程式表示加NaOH溶液的作用:()。
②用化学平衡原理解释通空气的目的:()。
问题二、过程Ⅱ:在微生物作用的条件下,NH经过两步反应被氧化成NO。两步反应的能量变化示意图如下:
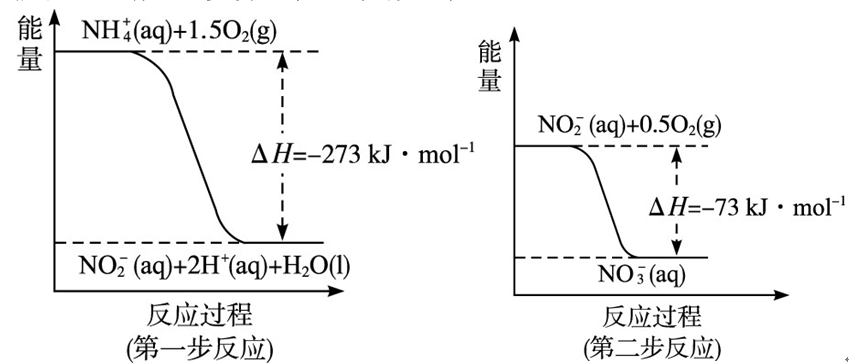
①第一步反应是()反应(选填“放热”或“吸热”),判断依据是()。
②1molNH(aq)全部氧化成NO(aq)的热化学方程式是()。
问题三、过程Ⅲ:一定条件下,向废水中加入CH3OH,将HNO3复原成N2。假设该反应消耗32gCH3OH转移6mol电子,则参加反应的复原剂和氧化剂的物质的量之比是()。
高铁酸钾是一种高效的多功能的水处理剂。工业上常采用NaClO氧化法生产,原理为:3NaClO+2Fe(NO3)3+10NaOH=2Na2FeO4↓+3NaCl+6NaNO3+5H2O Na2FeO4+2KOH=K2FeO4+2NaOH 主要的生产流程如下: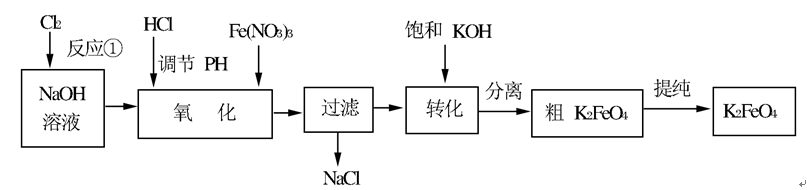 问题一、写出反应①的离子方程式()。
问题一、写出反应①的离子方程式()。
问题二、流程图中“转化”是在某低温下进行的,说明此温度下Ksp(K2FeO4)()Ksp(Na2FeO4)〔填“>”或“<”或“=”〕。
问题三、反应的温度、原料的浓度和配比对高铁酸钾的产率都有影响。
图1为不同的温度下,Fe(NO3)3不同质量浓度对生成率的影响;
图2为一定温度下,Fe(NO3)3质量浓度最正确时,NaClO浓度对K2FeO4生成率的影响
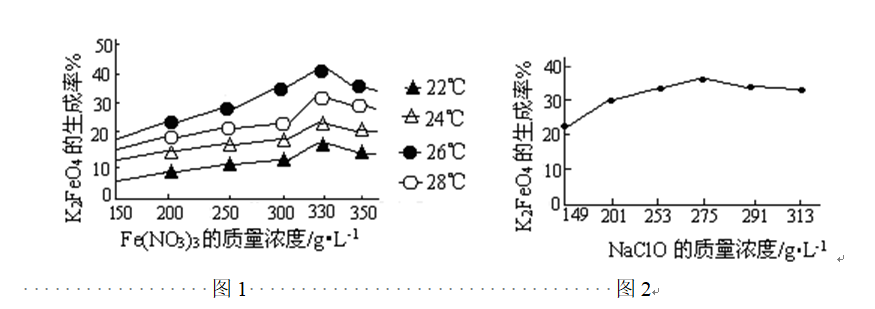
①工业生产中最正确温度为()℃,此时Fe(NO3)3与NaClO两种溶液最正确质量浓度之比为()。
②假设NaClO加入过量,氧化过程中会生成Fe(OH)3,写出该反应的离子方程式:()。假设Fe(NO3)3加入过量,在碱性介质中K2FeO4与Fe3+发生氧化复原反应生成K3FeO4,此反应的离子方程式:()。
问题四、K2FeO4在水溶液中易水解:
4FeO42—+10H2O 4Fe(OH)3+8OH—+3O2↑。在“提纯”K2FeO4中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用溶液()(填序号)。
4Fe(OH)3+8OH—+3O2↑。在“提纯”K2FeO4中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用溶液()(填序号)。
AH2O
BCH3COONa、异丙醇
CNH4Cl、异丙醇
DFe(NO3)3、异丙醇
工业上用铝土矿(主要成分为氧化铝,含少量氧化铁)制取铝的过程如图所示: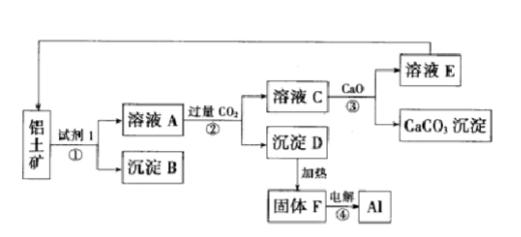 请回答:
请回答:
(1)试剂Ι为()(填化学式),①-④转化中属于氧化还原反应的是()(填序号);
(2)沉淀B的化学式为(),写出该物质发生铝热反应的化学方程式();
(3)电解F,当转移0.6mol,电子时,可制得铝()g;
(4)沉淀D是药物“胃舒平”的主要成分,可用于治疗胃酸(稀盐酸)过多,写出该反应的离子方程式();
(5)②中发生反应的离子方程式为()。


 如果结果不匹配,请
如果结果不匹配,请 
















