 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
已知反应在0.10mol·L-1Hg22+溶液中,有无Hg2+存在?说明Hg2卐
已知反应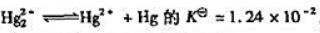 在0.10mol·L-1Hg22+溶液中,有无Hg2+存在?说明Hg22+溶液中能否发生歧化反应.
在0.10mol·L-1Hg22+溶液中,有无Hg2+存在?说明Hg22+溶液中能否发生歧化反应.
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知反应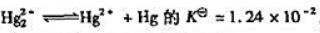 在0.10mol·L-1Hg22+溶液中,有无Hg2+存在?说明Hg22+溶液中能否发生歧化反应.
在0.10mol·L-1Hg22+溶液中,有无Hg2+存在?说明Hg22+溶液中能否发生歧化反应.
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知反应在0.10mol·L-1Hg22+溶液中,有无Hg2…”相关的问题
更多“已知反应在0.10mol·L-1Hg22+溶液中,有无Hg2…”相关的问题
A.0.51
B.0.45
C.0.15
D.0.13
已知298.15K时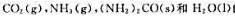 的标准摩尔生成焓和标准摩尔熵如下表所示:
的标准摩尔生成焓和标准摩尔熵如下表所示:

试通过计算判断下列反应
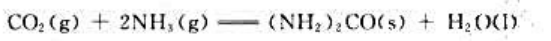
在298.15K、标准状态下能否自发进行。上述反应在标准状态下自发进行的最高温度是多少?
2N2H4(l)+N2O4(g)=3N2(g)+4H2O(g)
根据教材附录中的数据。计算反应在298K时的标准摩尔焓变 。若反应的热能完全转化为势能, 可将100kg的重物垂直升高多少?已知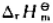 (N2H4,l)=50.63kJ·mol-1.
(N2H4,l)=50.63kJ·mol-1.
计算下列溶液的pH:
(1)0.10mol·L-1NaAc溶液;
(2)0.10mol·L-1NH4Cl溶液;
(3)0.010mol·L-1H2SO4溶液;
(4)0.10mol·L-1Na3PO4溶液;
(5)0.10mol·L-1NaH2PO4溶液;
已知298.15K时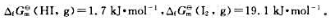 则化学反应
则化学反应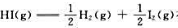 在298.15K时标准摩尔吉布斯自由能变
在298.15K时标准摩尔吉布斯自由能变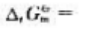 (),在标准状态下反应向方向自发进行。
(),在标准状态下反应向方向自发进行。
某温度下,反应
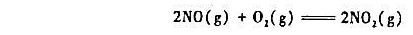
的速率常数k=8.8×10-2dm6·mol-2·s-1。已知此反应对O2是1级的,当两种反应物浓度都是 0.050mol-1·dm-3时,此反应的反应速率是多少?