 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
对于△H<0的反应2A(g)+B(g)⇌2C(g),增加压力使C、B、A的浓度均增加,正逆反应速率增加,但正反应速率增加的倍数大于逆反应增加的倍数,所以平衡向右移动。()
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“对于△H<0的反应2A(g)+B(g)⇌2C(g),增…”相关的问题
更多“对于△H<0的反应2A(g)+B(g)⇌2C(g),增…”相关的问题
A.ΔS>0,ΔH<0,任何温度下反应都能自发进行
B.ΔS<0,ΔH<0,低温有利于反应自发进行
C.ΔS<0,ΔH>0,任何温度下反应都是自发进行
D.ΔS>0,ΔH>0,低温下有利于反应自发进行
一定条件下,Ag与H2S可能发生下列反应: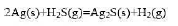 25°C,100kPa下,将Ag置于体积比为10:1的H2(g)与H2S(g)混合气体中。
25°C,100kPa下,将Ag置于体积比为10:1的H2(g)与H2S(g)混合气体中。
(1)Ag是否会发生腐蚀而生成Ag2S?
(2)混合气体中H2S气体的体积分数为多少时,Ag不会腐蚀生成Ag2S?
已知25°C时,H2S(g)和Ag2S(s)的标准生成吉布斯函数分别为-33.56kJ·mol-1和-40.26kJ·mol-1.
体(B)与NaOH共熔后溶于水生成绿色溶液(E),在(E)中加适量H2O2则生成黄色溶液(F)。将(F)酸化变为橙色溶液(G),在溶液(G)中加BaCl2溶液,得黄色沉淀(H)。在(G)的浓溶液中加KCl固体,溶解完全后,经蒸发、浓缩、冷却有橙红色晶体(I)析出。(I)受强热得到的固体产物中有(B),同时得到能支持燃烧的气体(J)。试给出(A),(B),(C),(D),(E),(F),(G),(H),(I)和(J)所代表的物质的化学式,并用化学反应方程式表示各过程。
某一位置随动系统,其开环传递函数为G(s)H(s)=K/s(5s+1),为了改善系统性能,分别采用在原系统中加比例及微分串联校正和速度反馈两种不同方案,校正前后的具体结构参数如图2-4-23所示。
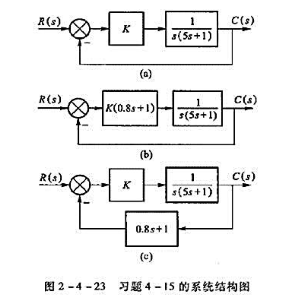
①试分别绘制这三个系统K从0→∞的闭环根轨迹图。
②比较两种校正对系统阶跃响应的影响。
设(X,Y)的联合分布律如下表所示, 0≤a≤0.4, 0≤ b≤0.4, a+b=0.4,则以下选项正确的是
0≤a≤0.4, 0≤ b≤0.4, a+b=0.4,则以下选项正确的是
A、X与Y不相关
B、Cov(X,Y)=0
C、X与Y独立当且仅当a=4/15
D、X与Y正相关
E、X与Y负相关
F、X与Y独立当且仅当a=0.25
G、E(X)= a当且仅当a=0.2
H、E(XY)=0.2
推理判断:
(1)将白色固体化合物(A)加热,生成(B)和(C)。白色固体(B)可以溶于稀盐酸生成(D)的溶液,再向其中滴加适量氢氧化钠生成白色沉淀(E),氢氧化钠过量时沉淀消失。(C)是(F)的酸酐,浓酸(F)与单质硫作用生成有刺激性气味的气体化合物(G)和水,稀酸(F)与金属锌作用生成化合物(A)。
试给出(A),(B),(C),(D),(E),(F)和(G)的化学式,并完成各步的化学反应方程式。
(2)向化合物(A)的水溶液中,通入硫化氢气体,生成黑色沉淀(B),(B)经过过氧化氢处理转化成(C)。离心分离后将白色沉淀物(C)加热分解,得到(D)和(E)。(D)与氧化钡反应生成白色固体(F),(F)不溶于水,也不溶于稀硝酸。(E)与稀硝酸反应又生成(A)。(A)受热分解得黄色固体化合物(E),
试给出(A),(B),(C),(D),(E)和(F)的化学式,并完成各步的化学反应方程式。
(3)向化合物(A)的水溶液中,滴加一种钠盐(B)的溶液,先生成白色沉淀(C),(B)的溶液过量时沉淀消失生成(D),继续加入少许盐酸,产生有刺激性气味的气体(E)和黑色沉淀(F),同时体系呈乳白色浑浊状,表示有单质(G)生成。离心分离后固体物质(F)和(C)一同与过量稀硝酸共热,形成的溶液比(A)的溶液多出一种离子(H),因此可以与氯化钡反应生成白色沉淀(I);向清液中加入氯化钡溶液,亦有(I)生成,(I)不溶于稀硝酸。白色沉淀(C)不稳定,与水共存时有(F)和(H)生成。
试给出(A),(B),(C),(D),(E),(F),(G),(H)和(I)的化学式,并完成各步的化学反应方程式。
A.活动bc1个星期,活动ef1个星期。
B.活动bc2个星期。
C.活动ef2个星期
D.活动ed1个星期,活动ef1个星期