 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知:C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1;2H2(g)+O2(g)=2H2O(l) ΔH=-483.6 kJ·mol-1。现有0.2 mol 的碳粉和氢气组成的悬浮气,该混合物在氧气中完全燃烧,共放出63.53 kJ热量,则混合物中C与H2的物质的量之比为()
A.1∶1
B.1∶2
C.2∶3
D.3∶2
 答案
答案
A、1∶1
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.1∶1
B.1∶2
C.2∶3
D.3∶2
 答案
答案
A、1∶1
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知:C(s)+O2(g)=CO2(g) ΔH=-393.5…”相关的问题
更多“已知:C(s)+O2(g)=CO2(g) ΔH=-393.5…”相关的问题
在汽车上安装三效催化转化器,可使汽车尾气中的主要污染物(CO、NOx、碳氢化合物)进行相互反应,生成无毒物质,减少汽车尾气污染。
问题一、已知:N2(g)+O2(g)=2NO(g)△H=+180.5kJ/mol2C(s)+O2(g)=2CO(g)△H=-221.0kJ/molC(s)+O2(g)=CO2(g)△H=-393.5kJ/mol尾气转化的反应之一:2NO(g)+2CO(g)=N2(g)+2CO2(g)△H=()
问题二、某研究性学习小组在技术人员的指导下,按以下流程探究某种催化剂在不同空燃比(空气与燃油气的质量比)条件下对汽车尾气的催化效果。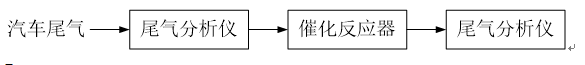
①实验过程中除空燃比不同外,其他条件:汽车尾气的流速、()等必须相同。
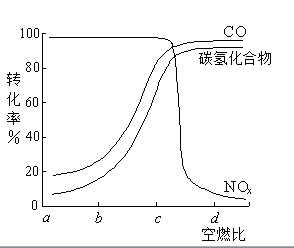
②在一定条件下,测得尾气中的主要污染物的转化率与空燃比的关系如右图所示。空燃比约为()时,催化剂对汽车尾气的催化效果最好。
问题三、CO分析仪以燃料电池为工作原理,其装置如下图,该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质NASICON中自由移动。以下说法错误的选项是()。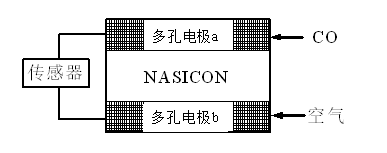
A负极的电极反应式为:CO+O2—―2e-=CO2
B工作时电极b作正极,O2-由电极a流向电极b
C工作时电子由电极a通过传感器流向电极b
D传感器中通过的电流越大,尾气中CO的含量越高
g)和H2O(l)。过程放热401.727kJ。求
压强变化不会使下列化学反应的平衡移动的是()。
A.Hz(g) +I2(g) ==2HI(g)
B.3H2(g) +N2(g) ==2NH3(g)
C.2SO2(g) +O2(g) ==2S03(g)
D.C(S) +CO2(g) ==2CO(g)
已知反应SnO2(s)+2H2(g)=Sn(s)+2H2O(g)和CO(g)+H2O(g)=CO2(g)+H2(g)的平衡常数分别为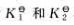 。则反应SnO2(s)+2CO(g)=2CO2(g)+Sn(s)
。则反应SnO2(s)+2CO(g)=2CO2(g)+Sn(s)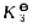 的=()。
的=()。
A.v(SO2)=4mol/(L·min)
B.v(O2)=0.05mol/(L·s)
C.v(SO3)=3mol/(L·min)
D.v(SO3)=0.05mol/(L·s)
A.SO2为0.4 mol,O2为0.2 mol
B.SO2为0.25 mol
C.SO2、SO3均为0.15 mol
D.SO3为0.4 mol
A.150
B.356
C.25
D.5.94
A.Fe+S=FeS△H=-95.6kJ/mol(反应热)
B.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=+57.3kJ/mol(中和热)
C.C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(g)△H=-1367.0kJ/mol(燃烧热)
D.S(s)+O2(g)=SO2(g)△H=-269.8kJ/mol(反应热)
A.Ag2O(s)=2Ag(s)+ O2(g)
O2(g)
B.N2O2=2NO2(g)
C.6C(s)+6H2O(g)=C6H12O6(s)
D.Fe2O3(s)+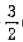 C(s)=2Fe(s)+
C(s)=2Fe(s)+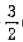 CO2g
CO2g
A.Na2O2遇到湿润的紫色石蕊试纸后,石蕊试纸最终变成蓝色
B.Na2O2与CO2反应生成0.1 mol O2时转移电子0.2 mol
C.Na2O2用于呼吸面具,活性炭用于防毒面具,两者原理相同
D.向饱和烧碱溶液中加入2 g Na2O2,充分反应完后,溶液中c(Na+)不变