 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
0.1000mol/LH2SO4标准溶液滴定20.00mLNaOH溶液,滴定至终点时用去此H2SO422.00mL,该NaOH溶液的浓度是()
A.0.2200mEq/L
B.2.200ml/L
C.0.2200mol/L
D.22.00mol/L
E.1.000mol/L
 答案
答案
C、0.2200mol/L
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.0.2200mEq/L
B.2.200ml/L
C.0.2200mol/L
D.22.00mol/L
E.1.000mol/L
 答案
答案
C、0.2200mol/L
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“0.1000mol/LH2SO4标准溶液滴定20.00mLN…”相关的问题
更多“0.1000mol/LH2SO4标准溶液滴定20.00mLN…”相关的问题
A.NH4Cl(Kb(NH3)=1.8×10-5)
B.H2SO4
C.HAc(Ka=1.8×10-5)
D.HCOOH(Ka=1.8×10-4)
A.15.77%
B.31.55%
C.47.32%
D.63.10%
A.V1>V2
B.V1=V2
C.V1 < V2
D.无法确定V1和V2的相对大小
A.水
B.较浓HC1溶液
C.较稀HC1溶液
D.标准溶液
MnO4-及MnO42-岐化生成的MnO4-和MnO2全部还原为Mn2+,剩余的Fe2+溶液用上述KMnO4标准溶液滴定至终点,消耗24.00mL.计算试液中HCOOH和HOAc的浓度各为多少?
用0.1000mol/LHCl溶液滴定0.1000mol/LNa2CO3溶液至pH5.00。计算有百分之几的Na2CO3变成了H2CO3?剩下的主要组分是什么?如果煮沸溶液以除尽CO2,冷却后溶液的pH为多少?(H2CO3的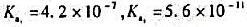 )
)
A.甲基橙
B.溴甲酚绿
C.酚酞
D.甲基红+溴甲酚绿