 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
若两电对在反应中电子转移数分别为1和2,为使反应完全程度达到99.9%,两电对的条件电势之差至少应大于( )。
A.0.09V
B.0.27V
C.0.36V
D.0.18V
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.0.09V
B.0.27V
C.0.36V
D.0.18V
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“若两电对在反应中电子转移数分别为1和2,为使反应完全程度达到…”相关的问题
更多“若两电对在反应中电子转移数分别为1和2,为使反应完全程度达到…”相关的问题
若两电对的电子转移数分别为1和2,为使反应完全度达到99.9%,两电对的条件电势差至少应大于( )
(A) 0.09V。 (B) 0.18V。 (C) 0.24V。 (D) 0.27V。
A.反应过程中,被氧化与被还原的元素的物质的量之比为1:2
B.NF3是一种无色、无臭的气体,因此NF3在空气中泄漏时不易被察觉
C.若反应中转移的电子数目为6.02×1023,则可生成22.4L NO气体(标准状况)
D.一旦NF3泄漏,可以用石灰水溶液喷淋的方法减少污染
标准状态下,由电对Ni2+/Ni和Pb2+/Pb组成电池。
(1)写出电池符号和电池反应方程式。
(2)计算电池电动势、电池反应的标准吉布斯自由能和平衡常数。
(3)在两电池溶液中同时加入S2-溶液,并使之都达到c(S2-)=1mol·L-1,求两电对的电极电势值,电池电动势和电池反应方向。
标准状态下,由电对Ni2+/Ni和Pb2+/Pb组成电池。
(1)写出电池符号和电池反应方程式。
(2)计算电池电动势、电池反应的标准吉布斯自由能和平衡常数。
(3)在两电池溶液中同时加入S2-溶液,并使之都达到c(S2-)=1mol·L-1,求两电对的电极电势值,电池电动势和电池反应方向。
如图,数轴上A,B两点对应的数分别为-4,-1。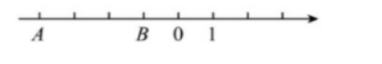 (1)求线段AB的长度。(2)若点D在数轴上,且DA=3DB,求点D对应的数。(3)若点A的速度为7个单位长度/秒,点B的速度为2个单位长度/秒,点O的速度为1个单位长度/秒,点A,B,O同时向右运动,几秒后,OA=3OB?
(1)求线段AB的长度。(2)若点D在数轴上,且DA=3DB,求点D对应的数。(3)若点A的速度为7个单位长度/秒,点B的速度为2个单位长度/秒,点O的速度为1个单位长度/秒,点A,B,O同时向右运动,几秒后,OA=3OB?
A.5
B.5.4
C.3.3
D.其它
A.氧化剂与还原剂的质量比为2∶1
B.氧化产物与还原产物的物质的量之比为2∶1
C.二氧化氮是氧化剂,水是还原剂
D.在反应中若有6 mol 二氧化氮参与反应时,有3 mol电子发生转移
某化学小组的同学为探究原电池原理,设计如图所示装置,将锌、铜通过导线相连,置于稀硫酸中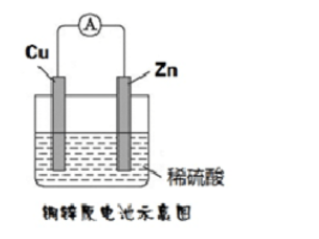 (1)外电路,电子从()极流出。溶液中,阳离子向()极移动。
(1)外电路,电子从()极流出。溶液中,阳离子向()极移动。
(2)若反应过程中有0.2mol电子发生转移,则生成的气体在标准状况下的体积为()。
(3)该小组同学将稀硫酸分别换成下列试剂,电流计仍会偏转的是()(填序号)。
A.无水乙醇
B.醋酸溶液
C.CuSo4溶液
D.苯
(4)实验后同学们经过充分讨论,认为符合某些要求的化学反应都可以通过原电池来实现。下列反应可以设计成原电池的是()(填字母代号)。
A.NaOH+HCl=NaCl+H2O
B.2H2+O2=2H2O
C.Fe+2FeCl3=3FeCl2
D.2H20=2H2↑+2O2↑
和齿数分别为:第一对m=4mm,z1=20,z2=40;第二对m'=2mm,z'1=40,z'2=80。若不考虑重合度不同产生的影响,试求在同样工况下工作时,这两款齿轮应力的比值σH/σ'H和σF/σ'F。
A.与NaOH反应的氯气一定为0.6 mol
B.n(Na+)∶n(Cl-) 可能为7:3
C.若反应中转移的电子为n mol,则0.3 n 0.5
D.n(NaCl)∶n(NaClO)∶n(NaClO3)可能为11∶2∶1
A.1可能大于G
B.2一定大于G
C.1一定大于F2
D.1一定等于F2