 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
某溶液中含有Fe3+和Fe2+,它们的浓度均为0.01mol·L-1,如果要求Fe3+沉
淀完全,而Fe2+不生成Fe(OH)3,问溶液的pH应控制在什么范围内?已知: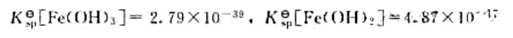
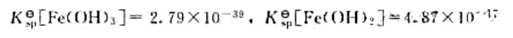
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
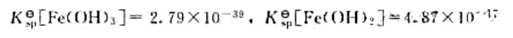
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“某溶液中含有Fe3+和Fe2+,它们的浓度均为0.01mol…”相关的问题
更多“某溶液中含有Fe3+和Fe2+,它们的浓度均为0.01mol…”相关的问题
A.=1
B.>1
C.<1
D.无法确定
298K时,在Fe3+,Fe2+的混合溶液中加入NaOH时,有Fe(OH)3和Fe(OH)2沉淀生成(假如没有其它反应发生)。当沉淀反应达到平衡时,保持c(OH-)=1.0molL-1,计算

准确称取铁矿石试样0.5000g,用酸溶解后加入SnCl2,使Fe3+还原为Fe2+,滴定Fe2+消耗24.50mLKMnO4标准溶液滴定,已知1mL.KMnO4相当于0.01260gH2C2O4·2H2O,(1)矿样中Fe及Fe2O3的质量分数各为多少?(2)取市售双氧水3.00mL,稀释定容于250.00mL,从中取出20.00mL试液,需用上述溶液KMnO421.18mL滴定至终点,计算每100.0mL市售双氧水所含H2O2的质量.
用KMnO4标准溶液滴定Fe2+的反应为:

试计算:①该反应的平衡常数;②为使反应完全定量进行(Fe2+≤10-3[Fe3+]),所需的最低[H+]是多少?(已知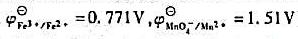 )
)
A.Mg2+ 量
B.Ca2+ 量
C.Ca2+、Mg2+ 总量
D.Ca2+、Mg2+ 、Fe3+、Al3+总量
A.Cu2+、Al3+的含量小于8mg/L。
B.Fe2+、Fe3+的含量小于8mg/L。
C.Zn2+、Mn4+的含量小于8mg/L。
D.Ca2+、Mg2+的含量小于8mg/L。