 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
由标准钴电极和标准氯电极组成原电池,测得其电动势为1.64 V,此时钴电极为负极。已知氯电极的标准
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“由标准钴电极和标准氯电极组成原电池,测得其电动势为1.64 …”相关的问题
更多“由标准钴电极和标准氯电极组成原电池,测得其电动势为1.64 …”相关的问题
由标准钴电极(Co2+/Co)与标准氯电极组成原电池,测得其电动势为1.64V,此时钴电极为负极。已知 (Cl2/Cl-)=1.36V。问:(1) 标准钴电极的电极电势为多少(不查表)?(2) 此电池反应的方向如何?(3) 当氯气的压力增大或减小时,原电池的电动势将发生怎样的变化?(4) 当Co2+的浓度降低到0.010mol·dm-3时,原电池的电动势将发生怎样的变化?数值是多少?
(Cl2/Cl-)=1.36V。问:(1) 标准钴电极的电极电势为多少(不查表)?(2) 此电池反应的方向如何?(3) 当氯气的压力增大或减小时,原电池的电动势将发生怎样的变化?(4) 当Co2+的浓度降低到0.010mol·dm-3时,原电池的电动势将发生怎样的变化?数值是多少?
某学生为测定CuS的溶度积常数,设计如下原电池:正极为铜片,在0.1mol·dm-3Cu2+的溶液中,再通入H2S气体使之达到饱和;负极为标准锌电极。测得电池电动势为0.670V。已知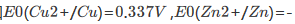 0.763V,H2S的
0.763V,H2S的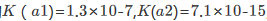 。试求CuS的溶度积常数。
。试求CuS的溶度积常数。
将反应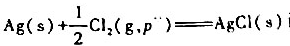 设计成原电池.已知25°C;时,
设计成原电池.已知25°C;时,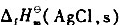 =-127.07kJ.mol-1.
=-127.07kJ.mol-1.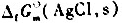 =-109.79kJ.mol-1,标准电极电势
=-109.79kJ.mol-1,标准电极电势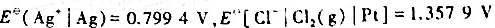 .
.
(1)写出电极反应和电池图示;
(2)求25°C、电池可逆放电2F电荷悬时的热Qz;
(3)求25°C时AgCl的活度积Kap.
A.X>Z>Y>W
B.Z>W>X>Y
C.Z>Y>X>W
D.Z>X>Y>W
A.锌为正极,Ag2O为负极
B.原电池工作时,负极区PH增大
C.原电池工作时,负极区PH增大,正极区PH减小
D.锌为负极:Zn+2OH--2e- =ZnO+H2O
酸度计测定溶液的pH值是基于参比电极和指示电极组成的化学原电池的电动势与溶液的()有关。
A.溶质浓度
B.溶质成分
C.溶剂的性质
D.氢离子的浓度
测定柠檬汁中氯化物含量时,用氯离子选择性电极和参比电极在100mL柠檬汁中测得电动势为-37.5mV,加入1.00mL1.0×10-2mol·L-1NaCl标准溶液,测得电动势为-64.9mV。已知MCl=35.45g·mol-1。计算柠檬汁中氯的含量,以mg·L-1表示。
A.它的最小单位称为原电池,是组成电池的重要组件
B.电池可以被当做一个电化学能转换系统,与内燃机类似
C.习惯上把原电池所具有的特性作为电池的特性
D.把化学能转换成机械能,完成这个过程需要两大物质:燃料和氧气
E.其中的一个电极使用金属物质,如锌、锂,在电解质中产生了负电压,代表负电极