更多“已知,但是Cu2+却能将I-化为I2,为什么?”相关的问题
更多“已知,但是Cu2+却能将I-化为I2,为什么?”相关的问题
第1题
已知电对的=1.3×10-12</sup>。(1)试求氧化还原反应298K时的平衡常数;(2)若溶液中Cu2+</sup>的
已知电对的=1.3×10-12</sup>。(1)试求氧化还原反应298K时的平衡常数;(2)若溶液中Cu2+</sup>的
点击查看答案
已知电对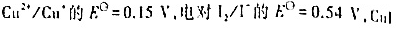 的
的
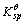 =1.3×10-12。
=1.3×10-12。
(1)试求氧化还原反应
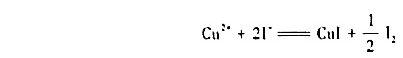
298K时的平衡常数;
(2)若溶液中Cu2+的起始浓度为0.10 mol·dm-3,I-的起始浓度为1.0 mol·dm-3,试计算达到平街时留在溶液中Cu2+的浓度。
第2题
设溶液中MnO4-和Mn2+浓度相等。根据(1)pH=3;(2)pH=6时的电极电势的计算结果判
设溶液中MnO4-和Mn2+浓度相等。根据(1)pH=3;(2)pH=6时的电极电势的计算结果判断MnO4-是否能把I-和Br-氧化成I2和Br2。已知: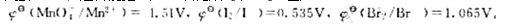
第3题
碘量法测定CuSO4含量,试样溶液中加入过量的KI,下列叙述其作用错误的是A.还原Cu2+为Cu+B.防止I2挥
碘量法测定CuSO4含量,试样溶液中加入过量的KI,下列叙述其作用错误的是
A.还原Cu2+为Cu+
B.防止I2挥发
C.与Cu+形成CuI沉淀
D.把CuSO4还原成单质Cu
第4题
间接碘量法中,将碘价瓶置于暗处是为了()。A.避免I2被歧化B.避免I-被氧化C.避免I2挥发D.保持低温
间接碘量法中,将碘价瓶置于暗处是为了()。
A.避免I2被歧化
B.避免I-被氧化
C.避免I2挥发
D.保持低温
第6题
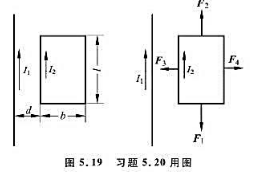
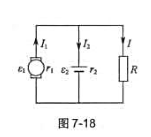
蓄电池ε2和电阻为R的用电器并联后接到发电机ε1的两端。如图7-18所示,箭头表示各支路中
的电流方向。已知ε2=108V,r1=0.40Ω, r2=0.2Ω,I2=10A,I1=25A。试确定蓄电池是在充电还是在放电?并计算ε1、I和R的值。
点击查看答案
第9题
298K时,铜片插入盛有1×10-8mol·L-1CuSO4溶液的烧杯中,锌片插入盛有1mol·L
-1ZaSO4溶液的烧杯中,电对Cu2+/Cu与Zn2+/Zn组成铜锌原电池, 已知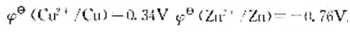 ,求此时原电池的电动势比标准状态时的电动势()
,求此时原电池的电动势比标准状态时的电动势()
点击查看答案
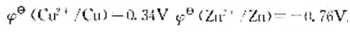 ,求此时原电池的电动势比标准状态时的电动势()
,求此时原电池的电动势比标准状态时的电动势()A.上升0.24V
B.下降0.24V
C.上升0.12V
D.下降0.12V

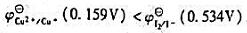 ,但是Cu2+却能将I-化为I2,为什么?
,但是Cu2+却能将I-化为I2,为什么?
 如果结果不匹配,请
如果结果不匹配,请