 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
某兴趣小组进行实验探究,向盛有硝酸亚铁和硝酸银混合液的烧杯中加入一定量的锌粉,反应停止后过滤,向滤渣中加入稀盐酸,有气泡产生下列说法正确的是()
A.滤液中一定含有Zn2+和Fe2+,一定没有Ag+
B.滤液中一定含有Zn2+,一定没有Fe2+和Ag+
C.滤渣中一定含有银,可能含有锌和铁
D.滤渣中一定含有银和铁,可能含有锌
 答案
答案
D、滤渣中一定含有银和铁,可能含有锌
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.滤液中一定含有Zn2+和Fe2+,一定没有Ag+
B.滤液中一定含有Zn2+,一定没有Fe2+和Ag+
C.滤渣中一定含有银,可能含有锌和铁
D.滤渣中一定含有银和铁,可能含有锌
 答案
答案
D、滤渣中一定含有银和铁,可能含有锌
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“某兴趣小组进行实验探究,向盛有硝酸亚铁和硝酸银混合液的烧杯中…”相关的问题
更多“某兴趣小组进行实验探究,向盛有硝酸亚铁和硝酸银混合液的烧杯中…”相关的问题
A.实验开始时,实验组和对照组的蝌蚪应大小相同
B.实验组和对照组的水温、水质及饵料等条件应一致
C.每组用一只蝌蚪进行一次实验,就可获得可靠的结果
D.实验结束后,应及时将实验动物放回适合它们生存的环境中
A.可以通过烟草浸出液对水蚤心率的影响的探究实验进行研究
B.选项A所指探究实验作出的假设只能是烟草浸出液会影响水蚤的心率
C.除了采用实验研究外,还可以采用调查法研究
D.通过调查研究发现,吸烟可能诱发肺癌
A.阴暗潮湿与阴暗干燥
B.阴暗潮湿与明亮潮湿
C.阴暗潮湿与明亮干燥
D.明亮湿润与明亮干燥
工业上以氨气为原料制备硝酸的过程如下: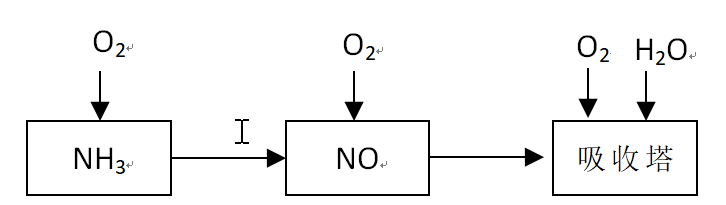 某课外小组模拟上述部分过程设计了如下实验装置制备硝酸(所有橡胶制品均已被保护)。
某课外小组模拟上述部分过程设计了如下实验装置制备硝酸(所有橡胶制品均已被保护)。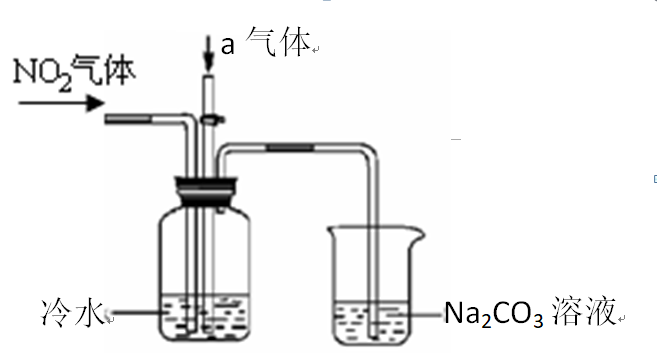
问题一、工业上用氨气制取NO的化学方程式是()。
问题二、连接好该装置后,首先进行的操作是()。
问题三、通入a气体的目的是()。
问题四、盛有Na2CO3溶液的烧杯为尾气处理装置,该装置中反应的化学反应方程式是2NO2+Na2CO3==NaNO2+()+()
问题五、已知:温度低于21.15℃时,NO2几乎全部转变为N2O4.工业上可用N2O4与水反应来提高硝酸产率。N2O4与a气体在冷水中生成硝酸的化学方程式是()。
问题六、一定条件下,某密闭容器中N2O4和NO2的混合气体到达平衡时,c(NO2)=0.50mol/L、c(N2O4)=0.125mol/L。则2NO2(g) N2O4(g)的平衡常数K=()。假设NO2起始浓度为2mol/L,相同条件下,NO2的最大转化率为()。
N2O4(g)的平衡常数K=()。假设NO2起始浓度为2mol/L,相同条件下,NO2的最大转化率为()。
A.滴加碘液后1号变蓝,2号不变蓝,此实验说明了唾液对淀粉有消化作用
B.滴加碘液后1号不变蓝,2号变蓝,此实验说明了水对淀粉有消化作用
C.滴加碘液后1号和2号均变蓝,此实验说明唾液对淀粉没有消化作用
D.滴加碘液后1号和2号不变蓝,此实验说明唾液和水对淀粉没有消化作用
A.由步骤(1)可知,白色粉末中一定含碳酸钠和氢氧化钙
B.步骤(2)结束后所得溶液中溶质除酚酞外,只有氯化钠和氢氧化钠
C.该白色粉末的组成可能是碳酸钠、氢氧化钙和碳酸钙
D.该白色粉末中可能含碳酸钙
A.①②④
B.②③④
C.①③④
D.①②③
A.①②④
B.②③④
C.①③④
D.①②③
A.①②④
B.②③④
C.①③④
D.①②③