 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
已知CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+206kJ/molCH4(g)+CO2(g)=2CO(g)+2H2(g)△H=+247kJ/molC—H键的键能约为413kJ/mol,O—H键的键能约为463kJ/mol,H—H键的键能约为436kJ/mol,则CO2中C=O键的键能约为()。
A.797.5kJ/mol
B.900.5kJ/mol
C.962.5kJ/mol
D.1595kJ/mol
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案


 更多“已知CH4(g)+H2O(g)=CO(g)+3H2(g)△H…”相关的问题
更多“已知CH4(g)+H2O(g)=CO(g)+3H2(g)△H…”相关的问题
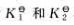 。则反应SnO2(s)+2CO(g)=2CO2(g)+Sn(s)
。则反应SnO2(s)+2CO(g)=2CO2(g)+Sn(s)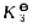 的=()。
的=()。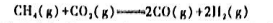
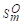 ,Δt
,Δt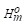 数据,求上述反应在25℃时的
数据,求上述反应在25℃时的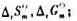
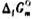 数据,计算上述及应在25℃时的
数据,计算上述及应在25℃时的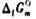 ;
;















