 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
已知25℃,φ°(MnO4-/Mn2-)=1.51V,当[MnO4-]=[Mn2-]=[H+]=0.10mo1/时,此电极电位值应为()V。
A.1.51
B.1.60
C.1.50
D.1.42
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.1.51
B.1.60
C.1.50
D.1.42
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知25℃,φ°(MnO4-/Mn2-)=1.51V,当[M…”相关的问题
更多“已知25℃,φ°(MnO4-/Mn2-)=1.51V,当[M…”相关的问题
设溶液中MnO4-和Mn2+浓度相等。根据(1)pH=3;(2)pH=6时的电极电势的计算结果判断MnO4-是否能把I-和Br-氧化成I2和Br2。已知: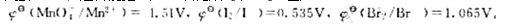
已知向量a =(3,4),b= (0, - 2),则 cos〈a,b〉=()。
A.4/5
B.-4/5
C.2/25
D.-2/25
已知向量a=(3,4),向量b=(0,-2),则cos<a,b>的值为()
A.4/5
B.-4/5
C.2/25
D.-2/25
已知数列{an}是等比数列,且a>0,a2a4+2a3a5+a4a6=25,那么a3+a5的值等于
A.5
B.10
C.15
D.20
已知25℃时Hg(l)的摩尔体积Vm=1.482x10-5m3·mol-1,体膨胀系数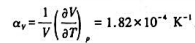 .恒温25℃时将1molHg(l)由100kPa加压到1100kPa,假设此过程Hg的体积变化可忽略不计,则过程的ΔS=()J·K-1.
.恒温25℃时将1molHg(l)由100kPa加压到1100kPa,假设此过程Hg的体积变化可忽略不计,则过程的ΔS=()J·K-1.
已知25°C时AgBr的活度积Kap=4.88x10-13,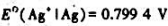 ,
,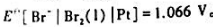 .试计算25℃时
.试计算25℃时
(1)银-溴化银电极的标准电极电势Eθ[Br-|AgBr(s)|Ag];
(2)AgBr(s)的标准摩尔生成吉布斯函数.
已知25℃时,液态水的标准摩尔生成吉布斯函数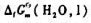 =-237.129kJ·mol-1,饱和蒸气压p''=3.1663kPa.求25℃时水蒸气的标准摩尔生成吉布斯函数.
=-237.129kJ·mol-1,饱和蒸气压p''=3.1663kPa.求25℃时水蒸气的标准摩尔生成吉布斯函数.