 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在下列物质中,属于晶体的是__;属于非晶体的是__;属于单晶体的是__;属于多晶体的是__.(填物质代号)()
A.玻璃
B.雪花
C.橡胶
D.铁块
E.单晶硅
F.沥青
 答案
答案
A、玻璃
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.玻璃
B.雪花
C.橡胶
D.铁块
E.单晶硅
F.沥青
 答案
答案
A、玻璃
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在下列物质中,属于晶体的是__;属于非晶体的是__;属于单晶…”相关的问题
更多“在下列物质中,属于晶体的是__;属于非晶体的是__;属于单晶…”相关的问题
A.在扩散运动中,只有注入的少子存在很大的浓度梯度,因此扩散电流主要是由少子贡献。
B.非晶硅对可见光谱的吸收很强,是晶硅的500倍,整个太阳光谱中的吸收系数也为单晶硅的40倍,因此非晶硅电池可做的很薄。
C.多晶硅和非晶硅电池都是由pn结构成的,因此它们的基本结构是相同的。
D.与晶体硅电池相比,非晶硅电池中存在光诱导退化效应(S-W效应),但其光电转化效率随温度升高下降较慢。
A.青蒿素属于脂溶性物质
B.青蒿素可以破坏疟原虫细胞的完整性
C.青蒿素可破坏疟原虫的细胞膜、核膜和细胞器膜
D.青蒿素的抗疟机理不会破坏线粒体的功能
已知NaCl的晶体结构如图C.17.1所示,它属于立方晶系,Oh点群。晶胞参数=564.0pm。
(I)写出通过晶胞中心的点对称元素。
(2)根据Na+和Cl-的离子半径值,了解在这结构中负离子是否接触?这种结构的稳定性如何?
(3)试计算NaCl晶体的密度D。
(4)将图C.17.1晶胞中顶角上的Na+和中心的Cl-除去,将Na+换成Nb2+,Cl-换得O2-即得NbO晶胞,试画出NbO的晶胞和其中原子簇的结构;已知晶跑参数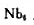 =421pm,计算晶体的密度i写出通过晶胞中心点的点对称元素和点群(Nb的相对原子质量为92.91);计算Nb2+的离子半径。
=421pm,计算晶体的密度i写出通过晶胞中心点的点对称元素和点群(Nb的相对原子质量为92.91);计算Nb2+的离子半径。
(5)将图C.17.1晶胞中面心和体心的原子除去,顶角上的Na+换成U6+,棱上的Cl-换成O2-,得UO3的晶体结构,立方晶胞参数a=415.6pm。试画出UO3晶胞的结构;写出通过晶胞中心点的点对称元素和点群;计算晶体的密度,计算U6+的离子半径(U的相对原子质量为238.0);画出由处在12条棱上的02-组成的立方八面体的图形;计算该多面体的自由孔径。