 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
℃,101.325kPa。NH3-H2O系统的平衡关系为y=2.74x,试求:(1)此塔中NH3的回收率为多大?(2)当吸收利用量为最小用量的2倍时,吸收剂用量和溶液出口浓度各为多少?
暂无答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“℃,101.325kPa。NH3-H2O系统的平衡关系为y=…”相关的问题
更多“℃,101.325kPa。NH3-H2O系统的平衡关系为y=…”相关的问题
A.101.325kpa,10℃
B.101.325kpa,15℃
C.101.325kpa,20℃
D.101.325kpa,25℃
已知水(H2O,I)在100℃的饱和蒸气压p=101.325kPa,在此温度.压力下水的摩尔蒸发焓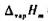 =40.668kJ·mol-1.求在100℃,101.325kPa下使1kg水蒸气全部凝结成液体水时的Q,W,ΔU和ΔH.设水蒸气适用理想气体状态方程.
=40.668kJ·mol-1.求在100℃,101.325kPa下使1kg水蒸气全部凝结成液体水时的Q,W,ΔU和ΔH.设水蒸气适用理想气体状态方程.
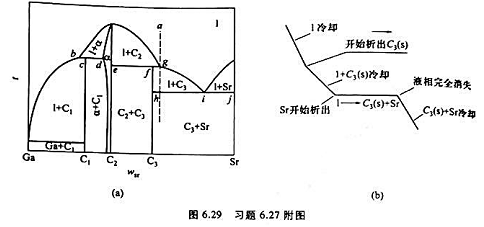
二组分凝聚系统Ga-Sr在101.325kPa下的相图见图6.29.
(1)标明C1,C2,C3,是稳定化合物还是不稳定化合物;
(2)标出各相区的稳定相,写出三相线上的相平衡关系;
(3)绘出图中状态点为a的样品的冷却曲线,并指明冷却过程相变化情况.
水中可溶解1.0g.如果用只能承受202.65kPa的瓶子充装溶有CO2(g)的饮料,则在20℃条件下充装时,CO2的最大压力为多少才能保证此瓶装饮料可以在40℃条件下安全存放?设CO2溶质服从亨利定律.
已知100°C水的饱和蒸气压为101.325kPa,此条件下水的摩尔蒸发焓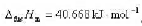 在置于100°C恒温槽中的容积为100dm3的密闭容器中,有压力120kPa的过饱和蒸气。此状态为亚稳态。今过饱和蒸气失稳,部分凝结成液态水达到热力学稳定的平衡态。求过程的Q,ΔU,ΔH,ΔS,ΔA及ΔG。
在置于100°C恒温槽中的容积为100dm3的密闭容器中,有压力120kPa的过饱和蒸气。此状态为亚稳态。今过饱和蒸气失稳,部分凝结成液态水达到热力学稳定的平衡态。求过程的Q,ΔU,ΔH,ΔS,ΔA及ΔG。
(1)101.325kPa下,与Na2CO3溶液及冰平衡共存的水合物最多能有几种?
(2)20℃时,与水蒸气平衡共存的水合物最多可能有几种?