 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
电池在25°C时测得电池电动势E=0.664V,试计算待测溶液的pH。
电池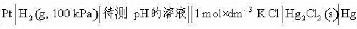 在25°C时测得电池电动势E=0.664V,试计算待测溶液的pH。
在25°C时测得电池电动势E=0.664V,试计算待测溶液的pH。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
电池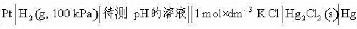 在25°C时测得电池电动势E=0.664V,试计算待测溶液的pH。
在25°C时测得电池电动势E=0.664V,试计算待测溶液的pH。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“电池在25°C时测得电池电动势E=0.664V,试计算待测溶…”相关的问题
更多“电池在25°C时测得电池电动势E=0.664V,试计算待测溶…”相关的问题
电池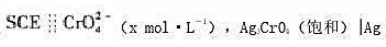 可用来测p(Cr04)。在25℃,若测得电池电动势为-0.386V,计算p(Cr04)。
可用来测p(Cr04)。在25℃,若测得电池电动势为-0.386V,计算p(Cr04)。
测得下列电池的电动势为0.873V(25℃)
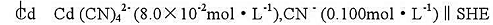
试计算Cd(CN)42-的稳定常数.
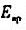 =0.82V。假设滴定过程中体积不变,求该有机酸的摩尔质量。
=0.82V。假设滴定过程中体积不变,求该有机酸的摩尔质量。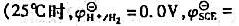
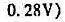
(1)写出电池反应方程式;
(2)由附表六查得Eθ(Cl2/Cl-),计算E(Co2+/Co);
(3)p(Cl2)增大时,电池的电动势将如何变化?
(4)当CO2+浓度为0.010mol·L-1其他条件不变时,电池的电动势是多少伏?
有如下两个电池:
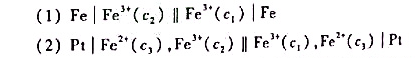
测得其电动势分别为E(1)和E(2),试求E(1)与E(2)之比。
丙烷燃料电池的电极反应为
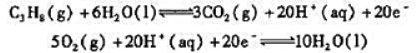
(1)指出正极反应和负极反应;
(2)写出电池反应方程式;
(3)计算25℃下丙烷燃料电池的标准电动势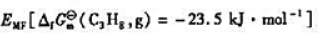
准确量取30.00ml弱酸,加水稀释至100ml。以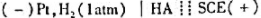 为测定电池,以0.1000mol/LNaOH溶液滴定弱酸HA。当酸被中和一半时,电池电动势为0.524V;化学计量点时,电池电动势为0.749V。φSCE=0.242V。计算:
为测定电池,以0.1000mol/LNaOH溶液滴定弱酸HA。当酸被中和一半时,电池电动势为0.524V;化学计量点时,电池电动势为0.749V。φSCE=0.242V。计算:
(1)弱酸HA的Ka。
(2)原弱酸HA的浓度。
下列电池
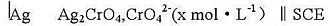
测得E=-0.285V,计算CrO42-的浓度(忽略液接电位).已知Ksp(Ag2CrO4)=9.0X10-12
已知下列原电池:
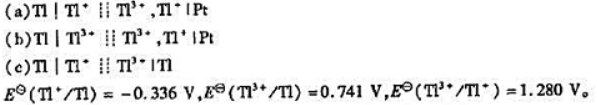
(1)写出各电池反应,并分别指出反应方程式中转移的电子数z;
(2)计算各电池的标准电动势EθMP;
(3)计算各电池反应的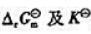 .
.
并联电池组的电动势等于()
A.各个电池电动势之和
B.各个电池电动势之差
C.各个电池电动势之积
D.一个电池的电动势